
| A. | 沼气和天然气都是不可再生的优质能源 | |
| B. | 图书、档案着火,用水基型灭火器灭火 | |
| C. | 发现家里的燃气泄漏,立即打电话报警 | |
| D. | 淡水资源约占全球水储量的2.53% |
分析 A、根据煤、石油、天然气都是化石燃料,属于不可再生的能源进行分析;
B、根据适用于用图书的灭火器材要考虑到不能造成二次损坏,应选用不会留下任何痕迹的灭火器进行分析;
C、根据可燃性气体与氧气或空气混合达到一定程度时,遇明火会发生爆炸进行分析;
D、根据可利用的淡水资源含量进行分析.
解答 解:A、煤、石油、天然气都是化石燃料,属于不可再生的能源,但沼气是可再生能源,故A错误;
B、水基型灭火器会对图书、档案造成损坏,故B错误;
C、天然气泄漏时,如果立即打电话报警,也可能发生爆炸,故C错误;
D、目前可利用的淡水资源约占全球水储量的2.53%,故D正确.
故选:D.
点评 化学来源于生产、生活,也服务于生产、生活,要学好化学知识,为生产、生活服务.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:初中化学 来源: 题型:选择题
| A. | 水受热变成水蒸气,水分子不变 | |
| B. | 氢气和液氢都可做燃料--相同物质的分子,其化学性质相同 | |
| C. | 变瘪的乒乓球放入热水中能鼓起来,是因为分子受热膨胀变大 | |
| D. | 用水银温度计测量体温--温度升高,原子间隔变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分别置于氧气中燃烧,都能得到一种产物CO2 | |
| B. | 观察它们的颜色来判断 | |
| C. | 测定三种物质的密度来判断 | |
| D. | 测定它们的硬度来判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
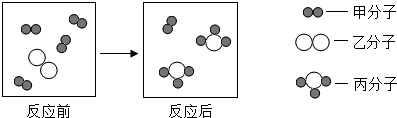
| A. | 参加反应的甲和乙分子个数比为4:1 | |
| B. | 该反应属于置换反应 | |
| C. | 反应前后原子的种类、数目都不变 | |
| D. | 反应前后各种元素的化合价都不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 预期现象和结论 |
| 1 | 各取2mL反应后的混合溶液分别加入A、B两只试管中 | 多余空 |
2 | 向A试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液 | 有气泡产生,品红溶液褪色,证明含有Na2SO3 |
3 | 向B试管中,加入足量的氯化钡溶液溶液,再加入足量的稀盐酸 | 先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有Na2SO4,则猜想3成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com