
分析 根据在金属活动性顺序表中,位于前面的金属能把位于后面的金属从它们的化合物溶液中置换出来,以及化学方程式的书写规则进行分析.
解答 解:熟记金属活动性顺序:钾K 钙 Ca 钠 Na 镁 Mg 铝 Al 锌Zn 铁Fe 锡Sn 铅Pb (H) 铜Cu 汞Hg 银Ag 铂Pt 金 Au.则:
(1)镁排在锌的前面,镁能与ZnCl2溶液反应,故Mg+ZnCl2=Zn+MgCl2;
(2)锌排在铁的前面,锌能与FeCl2溶液反应,故Zn+FeCl2=Fe+ZnCl2;
(3)铁排在铜的前面,铁能与CuSO4溶液反应,故Fe+CuSO4=Cu+FeSO4;
(4)铜排在银的前面,铜能与AgNO3溶液反应,故Cu+2AgNO3=2Ag+Cu(NO3)2.
故答案为:
(1)Mg+ZnCl2=Zn+MgCl2;
(2)Zn+FeCl2=Fe+ZnCl2;
(3)Fe+CuSO4=Cu+FeSO4;
(4)Cu+2AgNO3=2Ag+Cu(NO3)2
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义进行.解题的关键是掌握常见物质的性质及反应的条件.


科目:初中化学 来源: 题型:多选题
| 甲 | 乙 | 丙 |  |
 |  |  |
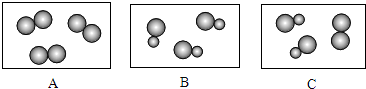
| A. | 物质甲的化学式是NH3 | |
| B. | 物质X的质量为2.8g | |
| C. | 物质X含两种元素 | |
| D. | 该反应化学方程式中物质X与O2的化学计量之比为3:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 茶氨酸由碳、氢、氧、氮四种元素组成 | |
| B. | 茶氨酸属于有机物,锌、硒指单质 | |
| C. | 一个茶氨酸妃子中含有3个氧原子 | |
| D. | 茶氨酸中氢元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事实 | 解释 |
| A | CO和CO2的化学性质不同 | 构成分子的原子的种类不同 |
| B | 氯化钠固体不导电,而氯化钠溶液能导电 | 构成氯化钠的粒子种类变化了 |
| C | 盐酸、硫酸显酸性 | 溶液中阳离子都只含有氢离子 |
| D | 水银温度计里的水银热胀冷缩 | 分子间的间隔随温度改变而改变 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
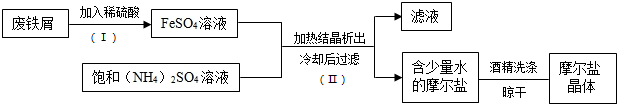

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 元素名称 | 钠 | 钙 | 铝 | 氢 | 氯 | 氧 | 硫 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
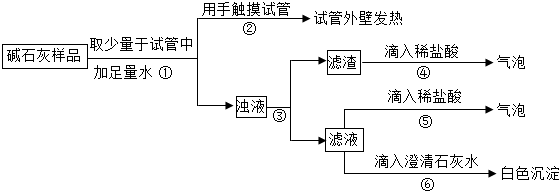
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com