
【题目】已确定某可燃性气体含有甲烷(CH4)和乙炔(C2H2),为进一步确定其组成,现取5.8g混合气体充分燃烧,测得生成CO2为17.6g,H2O为9g,则混合气体中CH4和乙炔C2H2的质量比为( )
A.13:23
B.16:13
C.3:8
D.13:8
【答案】B
【解析】解:将甲烷的化学式改写成CHH3 , 则混合气体中甲烷和乙炔碳元素和氢元素的原子个数比是1:1; 生成二氧化碳的质量是17.6g,则碳元素的质量是17.6g× ![]() =4.8g,设和碳元素结合的氢元素的质量为x
=4.8g,设和碳元素结合的氢元素的质量为x
C﹣﹣H
12 1
4.8g x![]() x=0.4g
x=0.4g
故混合气体中CH的质量和是:4.8g+0.4g=5.2g,故甲烷中H3的质量是5.8g﹣5.2g=0.6g,设甲烷中CH的质量是y
CH﹣﹣H3
13 3
y 0.6g![]() y=2.6g
y=2.6g
故甲烷的质量是2.6g+0.6g=3.2g,故乙炔的质量是5.8g﹣3.2g=2.6g
故甲烷和乙炔的质量比是3.2g:2.6g=16:13,观察选项,故选B.
根据质量守恒定律,化学反应前后元素的种类和原子的质量不变,将甲烷的化学式改写成CHH3进行解答即可.


科目:初中化学 来源: 题型:
【题目】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.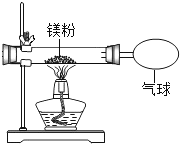
(1)请写出镁条与氧气反应的化学方程式 .
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我(填“同意”或“不同意”)小明的观点,因为 .
(3)小红同学按如图所示的装置改进实验,验证了质量守恒定律,却发现产物中还有少量淡黄色固体.
【提出问题】淡黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
实验操作 | 实验现象 | 结论 |
取少量黄色固体于试管中,加入适量的水,并将 . | 证明猜想正确 |
(4)【反思与交流】空气中N2的含量计远大于O22的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2 , 请给出合理的解释: . 写出生成Mg3N2的化学方程式 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海水中蕴含含有80多种元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氧气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.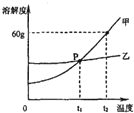
(1)氯碱工业中发生反应的化学方程式为:2NaCl+2H2O═2NaOH+Cl2↑+A,则A的化学式为 . 氯气常用于自来水的杀菌消毒,它与水反应生成盐酸和次氯酸(HClO),试写出该反应的化学方程式 .
(2)如图是甲、乙两种固体物质的溶解度曲线.
①P点的意义是 .
②甲物质中含有少量乙物质,提纯甲物质可用方法(选填“降温结晶”、“蒸发结晶”之一).请简述理由 .
③t2℃时,将100g固体甲与100g水混合后所得溶液的质量分数是 . (精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我们生活在不断变化的物质世界中,在下列变化中,有一个变化与其他变化有本质不同,该变化是( )
A.酒精燃烧
B.牛奶变酸
C.铁生锈
D.工业上从空气中分离出液态氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】意大利科学家获得了极具理论研究意义的N4分子,下列有关N4的说法正确的是( )
A.是一种新型的化合物
B.N4约占空气体积的78%
C.N4和N2的化学性质相似
D.一个N4分子中含有28个质子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com