
欲测定Cu﹣Zn合金及Cu﹣Ag合金中铜的 质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器。
质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器。
(1)你认为能测出铜的质量分数的是_________ 合金。
(2)取该合金的粉末32.5g与足量该硫酸充分反应,经测定产生了0.4g气体。
请你计算该合金中铜的质量分数。
【答案】(1)Cu﹣Zn(2)合金中铜的质量分数为60%
【解析】
试题分析:(1)在铜银合金中,两种金属的活动性 均在氢的后面。所以都不能和酸发生反应。因此无法测出其中的成分。在铜锌合金中,铜不与酸反应,锌能与酸反应生成氢气。所以可通过测量生成氢气的质量(或固体与酸充分反应后的减少的质量),得知金属锌的质量。进一步求出铜的质量分数。 即现有条件下能测出铜锌合金中铜的质量分数。
均在氢的后面。所以都不能和酸发生反应。因此无法测出其中的成分。在铜锌合金中,铜不与酸反应,锌能与酸反应生成氢气。所以可通过测量生成氢气的质量(或固体与酸充分反应后的减少的质量),得知金属锌的质量。进一步求出铜的质量分数。 即现有条件下能测出铜锌合金中铜的质量分数。
(2)已知量:氢气的质量为0.4g;未知量:铜在合金中的质量分数。
解题思路:可根据锌与硫酸反应的化学方程式,利用锌和氢气在反应中的质量关系求解出合金中含锌的质量。进一步求出铜的质量及其中合金中的质量分数。具体解题过程如下:
【解】设合金中Zn的质量为x。
Zn+H2SO4 ZnSO4+H2↑
65 2
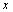 4g
4g
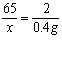
x = 13 g
合金中铜的质量= 32.5g – 13g = 19.5g
合金中铜的质量分数为: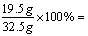 60%
60%
答:合金中铜的质量分数为60%。(其它合理解法均可)
考点:根据化学方程式的计算


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:
请根据物质的用途填空。
①活性炭 ②尿素 ③熟石灰 ④氧气
I.可作冰箱除味剂的是(1 ) (填序号,下同);
II.可作氮肥的是 ( 2 ) ;
III.能改良酸性土壤的是 ( 3 ) ;
IV.可供给呼吸的是 ( 4 ) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
某兴趣小组为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个 烧杯中分别加入11.0g样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体。
烧杯中分别加入11.0g样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体。
实验所得数据见下表,请你分析并进行有关计算:
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入氯化钙溶液的质量(g) | 50. | 110.0 | 150.0 |
| 白色固体的质量(g) | 5.0 | 10.0 | 10.0 |
(1)样品中碳酸钠的质量分数是多少?(结果精确到0.1%)
(2)求所加入的氯化钙溶液的溶质质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:
下列方法无法达到实验目的是( )
| A.用无色酚酞溶液鉴别稀盐酸和蒸馏水 B.用澄清石灰水鉴别氮气和二氧化碳 C.用肥皂水鉴别硬水和软水 D.用熟石灰中和废液中的盐酸
|
查看答案和解析>>
科目:初中化学 来源: 题型:
如图是甲、乙两种固体的溶解度曲线.下列说法中不正确的是
A.t1℃时,甲和乙的溶解度相等
B.t1℃时,30g乙加到100g水中形成饱和溶液
C.t2℃时,各100g饱和溶液降温至t1℃析出固体甲多于乙
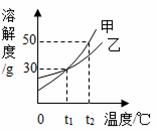 D.t2℃时,75g甲的饱和溶液中加100g水得到20%的溶液
D.t2℃时,75g甲的饱和溶液中加100g水得到20%的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com