
| A. | 如果合金为锌和铁,m可能是0.2g | |
| B. | 反应后溶液中的溶质只有两种 | |
| C. | 如果合金为锌和镁,m可能是0.1g,则该合金中锌的质量分数为50% | |
| D. | 如果合金为锌和铁,所加稀盐酸溶质质量分数一定大于7.3% |
分析 假设这6.5 g全部为锌,依据方程式计算出生成氢气为0.2g,所以剩余的金属中假设都是6.5g时产生氢气的质量必须有比0.2g大的,有比0.2g小的,然后结合金属与酸反应时生成氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量,再进行进一步分析即可.
解答 解:A、假设6.5g全部为锌,设生成氢气质量为x则:
Zn+2HCl═ZnCl2+H2↑
65 2
6.5g x
$\frac{65}{6.5g}=\frac{2}{x}$
解得:x=0.2g
同理可计算出6.5g铁与足量盐酸反应产生氢气的质量大于0.2g,
所以可以判断锌中含有铁,最终生成的氢气的质量都必然大于0.2g,故A正确;
B、如果盐酸过量的话,反应后的溶液中除了两种金属生成的盐溶质还有氯化氢,所以反应后溶液中的溶质可能有三种,故B错误;
C、有A分析可知,假设6.5g全部为锌,生成氢气质量为0.2g,同理可计算出若6.5g全部是镁,与足量盐酸反应产生氢气的质量大于0.2g,
所以可以判断如果锌中含有镁,最终生成的氢气的质量必然大于0.2g,如果合金为锌和镁,m不可能是0.1g,故C错误;
D、从上述方程式中可以分析得出,6.5g锌消耗盐酸的质量为7.3g,即此时盐酸的浓度为7.3%,等质量的铁消耗盐酸的质量更多,所以若混合物为锌和铁,则稀盐酸中溶质质量分数一定大于7.3%,故D正确.
故选:A、D.
点评 相同质量的金属与酸反应产生氢气的质量的多少与金属的相对原子质量和化合价有关,同价态的金属若相对原子质量越大,产生的氢气质量越小.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洗去试管壁上附着的铜:Cu+H2SO4═CuSO4+H2↑ | |
| B. | 镁带在空气中燃烧:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | |
| C. | 验证铁比铜活泼:Fe+CuSO4═FeSO4+Cu | |
| D. | 用熟石灰处理工业生产中含硫酸的废水;Ca(OH)2+H2SO4═CaSO4+2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
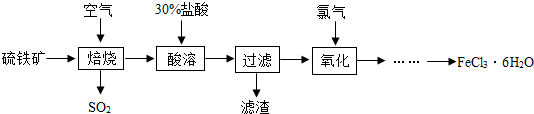
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
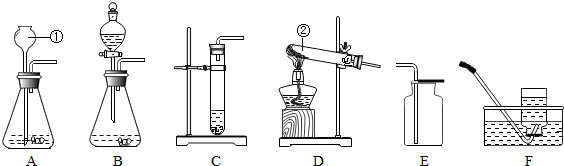
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是同学们在实验室制取气体,并进行气体的性质检测用到的仪器,请回答相关问题.
如图是同学们在实验室制取气体,并进行气体的性质检测用到的仪器,请回答相关问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
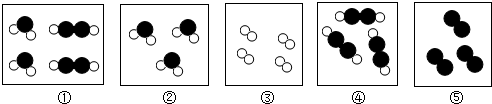
| A. | ①好②均为混合物 | B. | 只有③是单质 | ||
| C. | ①②④是氧化物 | D. | ④在一定条件下可分解成②和⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
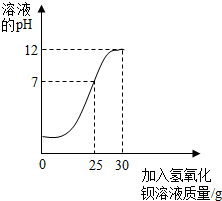 为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH的变化情况,过滤后得滤液47.67g.请你计算:
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH的变化情况,过滤后得滤液47.67g.请你计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com