
| A、原子中原子核内的质子数和中子数一定相等 |
| B、同种元素的原子和离子(如钠原子和钠离子)核外电子数相等 |
| C、参加化学反应的各物质的质量总和与反应后生成的各物质的质量总和相等 |
| D、参加化学反应的各物质的分子总数与反应后生成的各物质的分子总数相等. |


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:初中化学 来源: 题型:
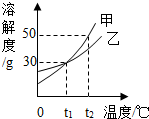
| A、t1℃时,甲和乙的溶解度相等 |
| B、t1℃时,30g乙加到100g水中形成饱和溶液 |
| C、分别将100g甲、乙的饱和溶液从t2℃降温到t1℃时,析出固体甲比乙多 |
| D、升高温度能使甲的不饱和溶液变为饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 ,其中X=
,其中X=查看答案和解析>>
科目:初中化学 来源: 题型:

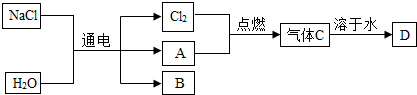
| A、图示中共有4种分子 |
| B、该反应属于分解反应 |
| C、该反应不符合质量守恒定律 |
| D、参加反应的物质均为化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com