

| 40 |
| 36.5 |
| x |
| 0.073g |
| 0.08g |
| 5g |


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:初中化学 来源: 题型:
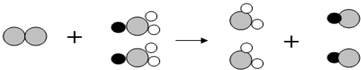
 氯原子,
氯原子, 表示钠原子,
表示钠原子, 表示氧原子)
表示氧原子)查看答案和解析>>
科目:初中化学 来源: 题型:

A、S+O2
| ||||
B、2H 2+O2
| ||||
C、2CO+O2
| ||||
D、CH4+O2
|
查看答案和解析>>
科目:初中化学 来源: 题型:
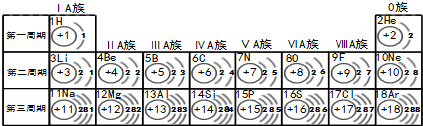
查看答案和解析>>
科目:初中化学 来源: 题型:
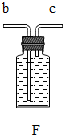 实验室用高锰酸钾加热制取氧气,有如下操作步骤:①加热;②检查装置的气密性;③装药品;④用排水法收集氧气;⑤从水槽中取出导管;⑥熄灭酒精灯;⑦连接装置.
实验室用高锰酸钾加热制取氧气,有如下操作步骤:①加热;②检查装置的气密性;③装药品;④用排水法收集氧气;⑤从水槽中取出导管;⑥熄灭酒精灯;⑦连接装置.查看答案和解析>>
科目:初中化学 来源: 题型:
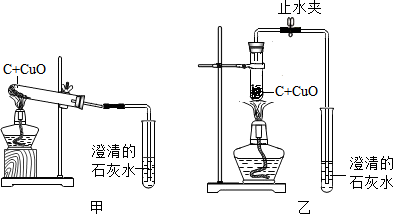 某中学化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.
某中学化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.查看答案和解析>>
科目:初中化学 来源: 题型:
| A、2Yg | B、Yg |
| C、(Y+1)g | D、(Y+2)g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com