
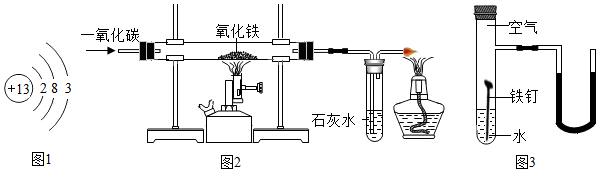
分析 (1)依据原子结构示意图的意义以及核外电子的得失规律和铝的有关性质分析解答;
(2)①根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳进行分析;
②根据一氧化碳在燃烧时产生蓝色火焰进行分析;
③根据一氧化碳有毒,要尾气处理进行分析;
④根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳进行分析;
(3)根据铁在潮湿的空气中会发生锈蚀进行分析;
(4)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,依据题中的数据进行计算.
解答 解:(1)A、根据原子结构示意图的特点可知:铝的核内质子数为13,故A正确;
B、根据原子的核外电子在化学反应中的规律特点可知:铝的最外层电子数是3,且在化学反应中易失掉3个电子而达到稳定结构,故B正确;
C、依据地壳中元素的含有情况可知,铝是地壳中含量最多的金属元素,而含量最多的元素是氧;故C错误;
D、根据金属铝的性质可知:铝具有较好的导电性,所以可以用铝制作导线;故D正确;
故选C;
(2)①一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,所以玻璃管中的现象是:红色粉末变成黑色;
②一氧化碳在燃烧时产生蓝色火焰,所以右边酒精灯上方的导管口有蓝色火焰出现;
③一氧化碳有毒,要尾气处理,所以右边酒精灯的作用是:除去未反应的CO,防止污染空气;
④一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)铁在潮湿的空气中会发生锈蚀,所以观察到的现象是:铁钉生锈,U形管液面变为左高右低;
(4)设生成硫酸亚铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 152
112g x
$\frac{56}{112g}$=$\frac{152}{x}$
x=304g
答:可生成硫酸亚铁304g.
故答案为:(1)C;
(2)①红色粉末变成黑色;
②蓝色火焰;
③除去未反应的CO,防止污染空气;
④Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)铁钉生锈,U形管液面变为左高右低;
(4)可生成硫酸亚铁304g.
点评 本题主要考查了学生对课本基本知识的掌握.学生在学习中要注意课本基础知识的复习、整理、理解,要在学习过程中学会向课本要答案.


 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:初中化学 来源: 题型:计算题
 实验室一瓶新购进的浓硫酸,其标签的部分内容如图所示.
实验室一瓶新购进的浓硫酸,其标签的部分内容如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
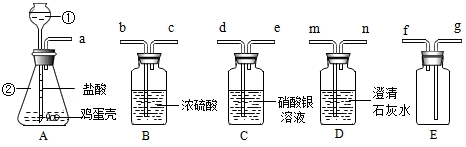
 已知A、B、C、D、E、F六种物质间有如图所示的转变关系(发生的反应都是化合反应),其中A、B、C在通常情况下是三种无色无味的气体,且C为化合物,D是一种无色的液体氧化物,F是一种能使紫色石蕊试液变红的物质.
已知A、B、C、D、E、F六种物质间有如图所示的转变关系(发生的反应都是化合反应),其中A、B、C在通常情况下是三种无色无味的气体,且C为化合物,D是一种无色的液体氧化物,F是一种能使紫色石蕊试液变红的物质.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A、化学与人体健康 | B、资源的利用和保护 |
| ①人体缺锌会导致甲状腺肿大 ②吸入一氧化碳会使人体中毒 | ①涂油漆、涂防锈油可防止金属锈蚀 ②石油是不可再生资源,只作燃料使用 |
| C、节能环保的措施 | D、垃圾的分类回收 |
| ①电器不使用时,及时拔掉插头 ②绿色植物既可保护水土又可制造氧气 | ①厨余垃圾、树叶等是有害垃圾 ②饮料瓶、易拉罐等是可回收垃圾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com