
| 实验 | 操作步骤 | 现象 | 结论 |
| 1 | 切开蜡烛,取出打火石,用砂纸打磨 | 打火石是银白色 | 该金属一定不是铜 |
| 2 | 取少量打磨后的打火石于试管中,滴加稀盐酸 | 金属溶解,有无色气体产生,溶液为无色 | 该金属一定不是铁 |
| 3 | 取少量打磨后的打火石于试管中,滴加适量硫酸铜溶液. | 有红色物质析出,溶液由蓝色变无色 | 该金属一定是镁 |
| 操作步骤 | 现象 | 结论 |
| 取少量打火石打磨后加入氯化铝溶液 | 有固体析出 | 这种金属是镁 |
分析 探究与反思:从题干信息对打火石的成分是合金进行分析,利用燃烧的条件判断灭火的方法.
实验探究:根据铜的颜色确定打火石是否属于铜,由于氯化亚铁的溶液是浅绿色的,所以采用打火石与盐酸的反应对反应后的溶液进行识别,溶液无色即为不是氯化亚铁的溶液.
分析思考:依据金属与盐溶液反应的规律:活动性排在前面的金属可以把后面的金属从其盐溶液中置换出来进行分析判断即可.
解答 解:探究与反思:利用燃烧的条件可知灯芯金属不燃烧是因为蜡蒸气起到了隔绝空气的作用,要想使其熄灭可控制燃烧的条件完成;
实验探究:打火石是银白色,而铜是紫红色的,所以该金属一定不是铜;根据氯化亚铁的溶液是浅绿色的事实分析可知:取灯芯加入盐酸如果生成无色的溶液则说明有没有铁存在;
分析思考:依据金属与盐溶液反应的规律是活动性强的金属可以从盐溶液中置换出活动性比它弱的金属分析可知:实验3中可能会发生Mg+CuSO4=MgSO4+Cu 也可能发生2Al+3CuSO4=Al2(SO4)3+3Cu,由于镁、铝、铜三种金属中铜的活动性最弱,所以镁与铝都可以置换出硫酸铜中的铜,因此不能证明该金属一定是镁也可能是铝,要想进一步判断可取少量打火石打磨后加入氯化铝溶液如有固体析出,则是镁,反之则是铝.或采用取剪除灯芯,在空气中点燃这种金属,发出耀眼的白光的是镁,不能点燃的是铝.
故答案为:
【探究与反思】蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以燃烧(只需答出“隔绝了氧气”或是“氧气不足”等意思即可);隔绝氧气或剪除灯芯或用湿抹布盖灭等;
【实验探究】实验1结论:该金属一定不是铜;
实验2操作步骤:取少量打磨后的打火石于试管中,滴加稀盐酸.
实验2现象:为无色.
【分析思考】
(1)Mg+CuSO4=MgSO4+Cu或2Al+3CuSO4=Al2(SO4)3+3Cu;
(2)铝也能与硫酸铜溶液反应,也有红色固体析出;
(3)取少量打火石打磨后加入氯化铝溶液如有固体析出,则是镁,反之则是铝.(或剪除灯芯,在空气中点燃这种金属,发出耀眼的白光的是镁,不能点燃的是铝.)
点评 此题是一道实验探究题,解题的关键是结合所学知识对个过程进行分析,从而设计正确的方法从而得到相应的结论.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:选择题
| A. | 16:9 | B. | 23:9 | C. | 32:9 | D. | 46:9 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
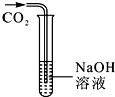 化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.
化学反应也有“悄悄”进行的.小明和他的同学对二氧化碳与氢氧化钠溶液的反应进行了如下探究.| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量试管中的溶液于试管中,加入足量CaCl2溶液,过滤;②向滤液中滴加适量酚酞试液 | 酚酞试液变红 | 小刚猜想成立 |
| 实验操作 | 实验现象 | 实验结论 | |
| 方案一 | 氢氧化钠和稀硫酸发生了反应 | ||
| 方案二 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加明矾,使海水中的盐分沉淀并淡化 | |
| B. | 利用太阳能,将海水蒸馏淡化 | |
| C. | 将海水通过离子交换树脂,以除去所含的盐分 | |
| D. | 利用半透膜,采用反渗透法而使海水淡化 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 假设 | 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
| ① | 取一定量粉末加入稀盐酸 | 没有气体产生 | 不成立 |
| ② | 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 成立 |
| ③ | 取一定量粉末溶于水,静置后取上层清液再通人二氧化碳 | 没有沉淀产生 | 不成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.| 实验步骤 | 实验现象 | 实验结论 |
| 你选用的试剂是: |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
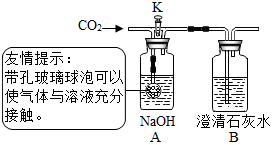 某探究小组的同学用如图所示实验装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.
某探究小组的同学用如图所示实验装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.| 实验步骤 | 实验现象 | 实验结论 |
| ①取滤液少许于管中,滴加Na2CO3溶液 | 无明显现象 | 猜想 三不成立 |
| ②重新取滤液少许于管中,滴入过量 氯化钙溶液,在滴入2~3滴无色酚酞 | 有白色沉淀生成,溶液变红色 | 猜想二成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
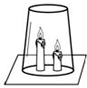 如图所示,将两支燃着的蜡烛罩上茶杯.试回答下列问题:
如图所示,将两支燃着的蜡烛罩上茶杯.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com