
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| NaOH的溶解度(g/100g水) | 42 | 109 | 129 | 174 | 314 | 347 |
| Ca(OH)2的溶解度(g/100g水) | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 |
| 实验步骤 | 实验现象 | 实验结论 |
| 甲同学:用一支洁净的试管取少量固体A,再加入过量稀盐酸. | 有气泡产生 | 自己的猜想 正确 |
| 乙同学:用一支洁净的试管取少量固体A,加水,充分振荡,向上层清液中滴加 |
上层清液由无色变为红色 | 自己的猜想 正确 |


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:初中化学 来源: 题型:
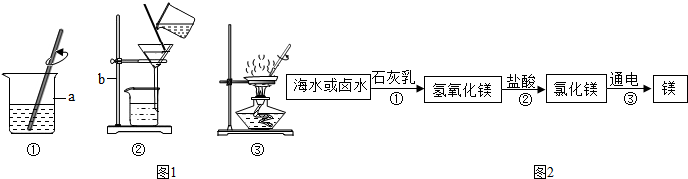
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验内容 |  |
 |
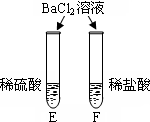 |
| 实验现象 | A试管内无明显现象,B试管中镁带表面观察到的现象是 |
C、D两试管中均观察到有气泡产生. | E试管中观察到的现象是 F试管中无明显现象. |
| 结论 | 酸的很多反应通常在水溶液中才能完成. | 不同的酸具有相似的化学性质. | 不同的酸根会导致酸的“个性”有差异. |
查看答案和解析>>
科目:初中化学 来源: 题型:
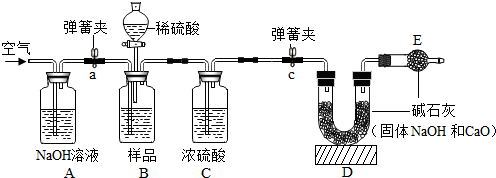
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
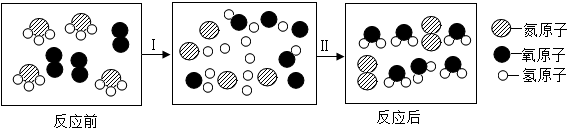
查看答案和解析>>
科目:初中化学 来源: 题型:
 A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):
A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com