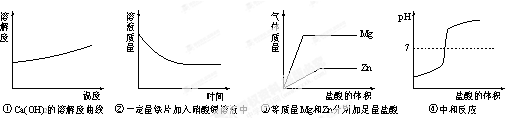
分析:①根据氢氧化钙溶解度受温度影响的情况进行分析;
②根据参加反应铁的质量与生成银的质量差进行分析;
③根据镁和锌的相对原子质量和金属活动性顺序进行分析;
④根据中和反应中pH的变化情况分析.
解答:解:①氢氧化钙的溶解度随温度的升高而降低,故①错误;
②铁和硝酸银溶液反应的过程中,溶液的质量减少,故②正确;
③由金属活动性顺序及镁和锌与酸反应生成氢气的速率和质量的关系可知,镁生成氢气的速率比锌要快,且生成氢气的质量多,故③正确;
④酸与碱起中和反应,碱溶液的pH是大于7的;溶液的pH应随盐酸的增加而逐渐降低,故④错误;
故选B.
点评:本题通过反应过程中曲线的变化,考查了物质溶解度,金属与酸反应,金属与盐反应,中和反应等多方面知识,对培养同学们对知识的整合能力和分析能力都很有帮助.