
| ||
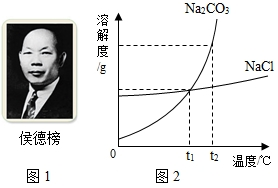
| 溶解度 |
| 100g+溶解度 |
| 溶解度 |
| 100g+溶解度 |


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?济南)世界上的物质丰富多样,有些物质能危害健康,现代社会中,毒品的危害并未完全消除,工农业生产带来的污染依然存在,香烟的产销量依然巨大.“珍爱生命,远离有毒物质”,是我们的一种生活理念,保护环境,建设和谐社会,实现“中国梦”,则是每个公民的责任.
(2013?济南)世界上的物质丰富多样,有些物质能危害健康,现代社会中,毒品的危害并未完全消除,工农业生产带来的污染依然存在,香烟的产销量依然巨大.“珍爱生命,远离有毒物质”,是我们的一种生活理念,保护环境,建设和谐社会,实现“中国梦”,则是每个公民的责任.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com