
分析 (1)根据铬和浓硫酸在加热的条件下生成硫酸铬、水和二氧化硫,以及化合价代数和为零进行分析;
(2)根据金属常见的物理性质进行分析;
(3)根据铬的硬度大,耐磨进行分析.
解答 解:(1)铬和浓硫酸在加热的条件下生成硫酸铬、水和二氧化硫,化学方程式为:2Cr+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Cr2(S04)3+3SO2↑+6H2O,反应前铬是单质,化合价是0价,反应后生成硫酸铬,硫酸根离子是-2价,所以铬显示+3价;
(2)该金属的物理性质是:银白色金属光泽的固体,有导电性,其导电性比铝弱;
(3)水龙头镀铬的具体原因是:铬的硬度比铁大,耐磨,美观又防锈,可以延长水龙头的使用寿命.
故答案为:(1)2Cr+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Cr2(S04)3+3SO2↑+6H2O;0价、+3价;
(2)银白色金属光泽的固体,有导电性,其导电性比铝弱;
(3)铬的硬度比铁大,耐磨,美观又防锈,可以延长水龙头的使用寿命.
点评 本题主要考查铬的物理性质和化学性质,难度不大,认真分析题意即可完成.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
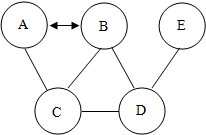 推断如图所示,其中A、B、C、D、E分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、二氧化碳中的一种.两圆连线表示二者可以发生反应.已知A和B可以通过反应相互转化.请回答下列问题:
推断如图所示,其中A、B、C、D、E分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、二氧化碳中的一种.两圆连线表示二者可以发生反应.已知A和B可以通过反应相互转化.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 细铁丝在氧气中燃烧的现象为:剧烈燃烧,火星四射,生成四氧化三铁 | |
| B. | 硫在氧气中燃烧,发出蓝紫色火焰 | |
| C. | 油锅着火,可用锅盖盖灭,依据的灭火原理是隔绝空气 | |
| D. | 氧气能与大多数的金属、某些化合物反应,化学性质比较活泼 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
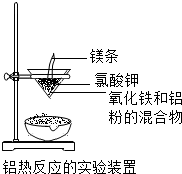 铝热法可简单认为是铝与某些金属氧化物(如Fe2O3、Fe3O4、Cr2O3等)在高热条件下发生的反应.铝热反应常用于冶炼高熔点的金属,并且它是一个放热反应.
铝热法可简单认为是铝与某些金属氧化物(如Fe2O3、Fe3O4、Cr2O3等)在高热条件下发生的反应.铝热反应常用于冶炼高熔点的金属,并且它是一个放热反应.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2、N2 | B. | N2 | C. | CO2、N2 | D. | CO、N2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com