
分析 硫酸钠不能和氢氧化钠反应,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,根据提供的数据可以计算氢氧化钠、硫酸镁、生成的硫酸钠等物质的质量,进一步可以计算混合物中硫酸镁的质量分数和加入氢氧化钠溶液的溶质质量分数.
解答 解:(1)设氢氧化钠的质量为x,硫酸镁的质量为y,生成硫酸钠质量为z,
2NaOH+MgSO4=Na2SO4+Mg(OH)2↓,
80 120 142 58
x y z 2.9g
$\frac{80}{x}=\frac{120}{y}=\frac{142}{z}=\frac{58}{2.9g}$,
x=4g y=6g z=7.1g
混合物中硫酸镁的质量分数为:$\frac{6g}{8g}$×100%=75%,
答:混合物中硫酸镁的质量分数为75%.
(2)设氢氧化钠溶液的质量为m,
根据题意有:(m+8g-2.9g)×10%=(8g-6g)+7.1g
m=85.9g,
加入氢氧化钠溶液的溶质质量分数为:$\frac{4g}{85.9g}$×100%=4.7%,
答:加入氢氧化钠溶液的溶质质量分数为4.7%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:解答题
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下一氧化碳能还原氧化铁生成铁 | Ⅰ对;Ⅱ对 |
| C | 铁比铝更易锈蚀 | 铝比铁活泼 | Ⅰ错;Ⅱ对 |
| D | 铝在空气中表面生成致密氧化膜 | 不能用铝罐储存运输稀硫酸、稀盐酸 | Ⅰ错;Ⅱ对 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
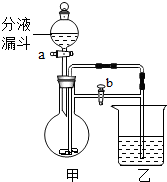 化学小组同学利用如图装置进行相关实验.
化学小组同学利用如图装置进行相关实验.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com