
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
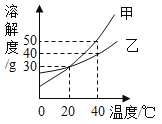
A. 甲的溶解度大于乙的溶解度
B. 将40℃甲的饱和溶液降温至20℃,溶液质量不变
C. 40℃时,分别在100g水中各加入30g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液
D. 20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数
 教学练新同步练习系列答案
教学练新同步练习系列答案科目:初中化学 来源: 题型:
【题目】探究碳酸氢钠、碳酸钠分别与稀盐酸反应,研究小组进行如下两个实验:
(1)(实验1)同时将足量的稀盐酸倒入锥形瓶甲和锥形瓶乙中。
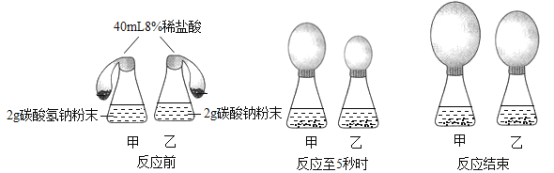
反应至5s生成气体的速率;碳酸氢钠_____碳酸钠(选填“>”,“<”,“=”)。
(实验2)分别将足量的稀盐酸逐滴滴入试管甲和试管乙中,边滴边振荡。
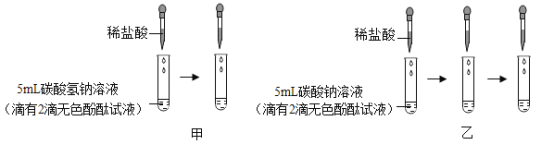
现象为:
①试管甲中的溶液开始时显浅红色,逐滴滴入稀盐酸立即产生大量气泡,浅红色逐渐消失。
②试管乙中的溶液开始时显红色,滴入稀盐酸没有气泡产生,溶液颜色逐渐变为浅红色后,继续滴加稀盐酸有大量气泡产生,浅红色逐渐消失。
(2)(反思1)在(实验2)碳酸钠溶液中逐滴滴入稀盐酸,为何刚开始没有大量气泡产生?研究小组查阅资料,绘制出微观示意图。
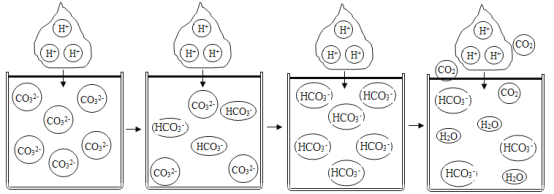
①碳酸钠溶液中逐滴滴入稀盐酸,依次发生反应的化学方程式为_____、_____
②相同浓度的碳酸氢钠溶液和碳酸钠溶液的碱性;碳酸氢钠_____碳酸钠(选填“>”,“<”,“=”)。
③若定量比较碳酸氢钠和碳酸钠酸碱性强弱,则需测定它们的pH值,所用到的玻璃仪器是_____,其作用为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】掌握科学的研究方法,探索化学世界的奥秘。
(1)分类是学习化学的重要方法之一,生活中,常会接触到下列物质:
A 钢丝 B 甲烷 C 生石灰 D 碘酒
其中属于混合物的是_____(填字母,下同),属于氧化物的是_____。
(2)实验室中可用KClO3在MnO2催化下受热分解制取氧气,化学方程式为_____,将反应后的混合物进行分离。实验操作如图所示:
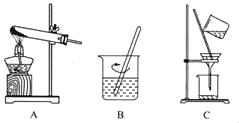
①图A中试管口略向下倾斜的原因是_____;
图B操作中玻璃棒的作用是_____;
图C操作中的一处明显错误是_____。
(3)质量守恒定律是帮助我们认识化学反应实质的重要理论。①下列表述正确的是_____。
A 蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B 每32gS和32gO2完全反应后,生成64gSO2
C 在化学反应aA+bB═cC+dD中一定有:a+b=c+d
②化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如表:
R | O2 | CO2 | H2O | |
反应前质量/g | 46 | 128 | 0 | 0 |
反应后质量/g | 0 | 32 | x | 54 |
若参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙烯(C2H4)是制塑料的主要原料,其分子结构如图所示,下列关于乙烯分子叙述正确的是( )
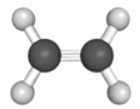
A. 它是由碳元素和氢元素组成的化合物
B. 它由2个碳原子和4个氢原子构成的
C. 其中含有的质子数一定等于电子数
D. 其中氢原子和碳原子的个数比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图为初中化学常见物质A、B、C、D、氢氧化钠和稀硫酸之间的反应及转化关系图(物质是溶液的只考虑溶质)。图中用“﹣”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质(部分反应物或生成物及反应条件已略去)。A是一种黑色粉末,B的溶液呈蓝色,B、C中含一种相同元素,D可以用于制玻璃。
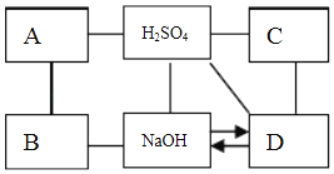
(1)请分别写出A和C物质的化学式:A._____ C._____;
(2)写出反应关系中有白色沉淀生成的反应化学方程式:_____、_____;
(3)写出A和B溶液反应的实验现象:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究酸碱中和反应是否放热,某同学设计了如图所示的实验装置(夹持等固定装置图略),针对该实验目的,下列评价或改进,错误的是

A.若观察到红墨水向右移,则说明该实验一定有放热现象
B.为了使实验现象更明显,可改用氢氧化钠固体
C.在打开活塞a之前应先打开橡皮管上的止水夹
D.为了使实验更具有说服力,可用氢氧化钾溶液再次实验
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( )
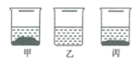
A. 所得溶液可能都是饱和溶液
B. 20℃时,乙溶液的溶质质量最小
C. 溶液溶质的质量分数:甲>丙>乙
D. 升高温度,溶液溶质的质量分数一定变大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有铜和氧化铜的固体混合物粉末,为研究其组成情况,进行如下实验,请回答下列问题:
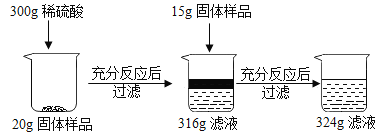
(1)上述实验过程中发生反应的化学方程式为______。
(2)样品中单质Cu的质量分数是______;
(3)第一次反应后所得316g滤液中的溶质是______
(4)根据已知条件列出求解300g稀硫酸中溶质质量(X)的比例式______。
(5)若向最终滤液中加入76g水,所得不饱和溶液中溶质的质量分数为_____
(6)配制上述所需的稀硫酸,需要质量分数为98%的浓硫酸和水的质量比是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应).课外小组为了测定该石灰石样品中碳酸钙的质量分数,将一定量的石灰石样品放入烧杯中,再取100g稀盐酸分4次加入烧杯中,每次均充分反应.实验数据记录如下:
次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
反应后烧杯中物质的总质量/g | 35.2 | 58.4 | 82.6 | 107.6 |
求:
(1)第1次加入稀盐酸充分反应后,生成二氧化碳的质量是_____g.
(2)该石灰石样品中碳酸钙的质量分数_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com