
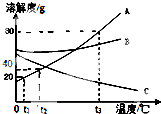
 根据A、B、C 三种固体物质的溶解度曲线回答:
根据A、B、C 三种固体物质的溶解度曲线回答:| 100g |
| X |
| 80g |
| 100g |
| Y |
| 125g |
| 40g |
| 100g |
| 20g |
| 20g+100g |


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:初中化学 来源: 题型:
| A、四氧化二氮属于非金属氧化物 |
| B、液氧为无色液体 |
| C、偏二甲肼中氢、氮元素的质量比为2:7 |
| D、每个偏二甲肼分子由2个碳原子、8个氢原子和2个氮原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:
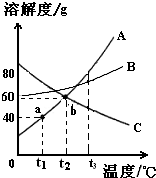 曲线A、B、C分别代表三种固体物质的溶解度曲线,根据图示回答:
曲线A、B、C分别代表三种固体物质的溶解度曲线,根据图示回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
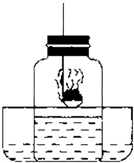 我们已经知道了空气的主要成分是氮气和氧气,如图为测定空气中氧气含量的实验装置图.
我们已经知道了空气的主要成分是氮气和氧气,如图为测定空气中氧气含量的实验装置图.| 1 |
| 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 生命必需的水在化学中常用作溶剂和原料.
生命必需的水在化学中常用作溶剂和原料.查看答案和解析>>
科目:初中化学 来源: 题型:
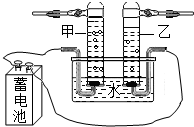
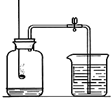 为了测定空气的成分,同学们按如图装置进行了实验.
为了测定空气的成分,同学们按如图装置进行了实验.| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 现象 | 结论 |
| 情况①正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com