
分析 【锌的广泛应用】
(1)根据常见元素对人体健康的影响分析;
(2)根据实验室氢气制取书写对应的化学方程式;
【制备七水硫酸锌】
根据给出的七水硫酸锌的制备流程结合给出的问题进行分析,而不要只是从流程图分析.
【组成测定】
根据给出的数据分析计算.最后的化学方程式注意配平即可
解答 解:
【锌的广泛应用】
(1)缺乏锌元素时,会导致“侏儒症”和智力发育不良. 补“锌”采用药补与食补并举,经常吃贝壳类海产品、红色肉类等含锌的食物有利补“锌”,这个“锌”是强调含有什么,而不是具体以什么形式存在,所以统称为元素.
(2)实验室用锌与稀硫酸制取氢气,同时得到副产品硫酸锌.反应物为锌和硫酸,生成物为硫酸锌和氢气,对应的化学方程式为 Zn+H2SO4═ZnSO4+H2↑.
【制备七水硫酸锌】
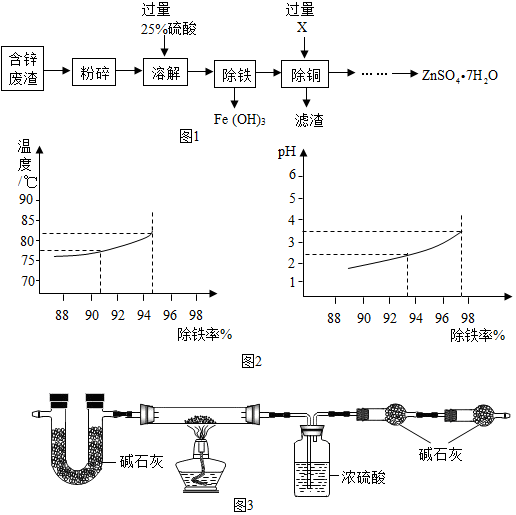
以含锌废渣(主要成分为ZnO,杂质为FeO﹑CuO)为原料制备七水硫酸锌(ZnSO4•7H2O)的流程如图1所示.是主要成分为ZnO,杂质为FeO﹑CuO和过量的六三反应得到硫酸锌、硫酸亚铁和硫酸铜的混合溶液,除铁是将可溶性铁盐转化为氢氧化铁沉淀,此处进一步过滤,得到含有硫酸锌和硫酸铜以及剩余的硫酸的混合溶液,加入过量X,此时是除铜,为避免引入新的杂质,所以就应该加入锌,由于加入的锌是过量的,所以滤渣含有铜和剩余的锌.
而除铁根据给出的除铁率与温度和pH的关系图选择温度在83℃和pH为3.5左右除铁率最高.根据曲线图本身的数据误差,此处数据允许有偏差.
(1)粉碎的目的是 增大接触面积,使反应更快更充分.
(2)若实验室用质量分数为98%,密度为1.84g/ml的浓硫酸配制200g、25%的稀硫酸,
根据溶液稀释过程中溶质的质量保持不变.设需要的浓硫酸的体积为x.
98%×1.84g/mLx=200g×25%
x≈27.7mL
配制时,需要的玻璃仪器有量筒﹑玻璃棒、烧杯和 胶头滴管,
(3)物质X是 Zn,滤渣中含有的金属单质有 Zn和Cu,
(4)流程中获得七水硫酸锌前省略的操作是 蒸发浓缩﹑冷却结晶﹑过滤、洗涤和低温烘干.
(5)某温度下,Fe(OH)3分解得到一种铁﹑氧质量比21:8的氧化物,设对应的化学式为FeaOb.
根据铁﹑氧质量比21:8,可得$\frac{a}{b}$=$\frac{\frac{21}{56}}{\frac{8}{16}}$=$\frac{3}{4}$,所以该氧化物的化学式 Fe3O4.
(6)除铁过程中,温度、pH对除铁效果的影响分别对如图所示.由图2可知,除铁时温度应控制在 83±1℃为宜,pH应控制在 3.5±0.1为宜(此处数据偏差不超过上下限即可).
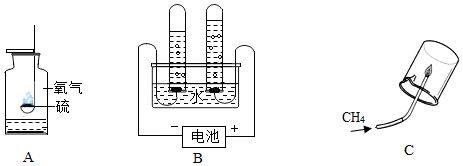
【组成测定】因为是通过装置CD进行二氧化碳和水的质量确定成分,所以首先要避免空气中二氧化碳和水的干扰,所以A装置是除去空气中的二氧化碳和水的干扰.E装置是避免右侧的空气中的二氧化碳造成干扰的,否则会导致测得的二氧化碳偏高.
现称取35.9g aZnCO3•bZn(OH)2•cH2O在B装置中进行煅烧,将完全煅烧过程中产生的气体依次通过装置C和装置D,它们分别增重7.2g和4.4g,则氧化锌的质量为35.9g-7.2g-4.4g=24.3g.
aZnCO3•bZn(OH)2•cH2O $\frac{\underline{\;高温\;}}{\;}$(a+b)ZnO+(b+c)H2O+aCO2↑
(a+b):(b+c):a=$\frac{24.3g}{81}$:$\frac{7.2g}{18}$:$\frac{4.4g}{44}$
a:b:c=1:2:2.
【实验分析及数据处理】
(1)装置A的作用是 除去空气中的CO2 和H2O.
(2)若没有E装置,测得二氧化碳的质量 偏大(填“偏大”、“偏小”或“无影响”).
(3)根据上述数据,化学式a ZnCO3•b Zn(OH)2•c H2O中的a:b:c=1:2:2.
【反思与拓展】
滤渣成分因温度等不同导致a、b、c会有差异,假设B化学式为ZnCO3•2Zn(OH)2•H2O,向该B中加入稀硫酸,生成硫酸锌和水以及二氧化碳,配平的时候先设定ZnCO3•2Zn(OH)2•H2O的系数为1,则对应的化学方程式为:ZnCO3•2Zn(OH)2•H2O+3H2SO4=3ZnSO4+6H2O+CO2↑.
故答案为:
【锌的广泛应用】
(1)侏儒; B;(2)Zn+H2SO4═ZnSO4+H2↑;
【制备七水硫酸锌】
(1)增大接触面积,使反应更快更充分;(2)27.7mL; 胶头滴管;
(3)Zn; Zn、Cu;(4)蒸发浓缩; (5)Fe3O4;
(6)83±1; 3.5±0.1;
【组成测定】
(1)除去空气中的CO2 和H2O;(2)偏大;
(3)1:2:2;
(4)ZnCO3•2Zn(OH)2•H2O+3H2SO4=3ZnSO4+6H2O+CO2↑.
点评 归纳类的题目解答不要从题干区分析解答,而是先研究需要回答的问题,从问题去寻找题干中解答可能用到的信息和线索.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
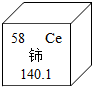 铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )
铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )| A. | 原子核内质子数为58 | B. | 属于非金属元素 | ||
| C. | 相对原子质量140.1g | D. | 原子核内中子数为58 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
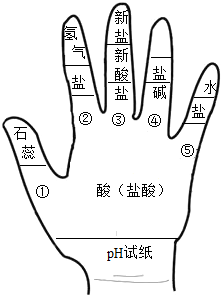 构建模型和构建知识网络是化学学习中重要的学习方法,某同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,某同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
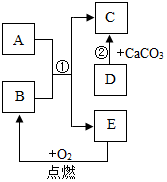 初中化学常见物质A-E有如图所示的转化关系(部分反应条件及物资已略去),已知A为单质,C为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位.
初中化学常见物质A-E有如图所示的转化关系(部分反应条件及物资已略去),已知A为单质,C为气体,反应②为实验室制取气体C的方法;E元素在地壳中含量居金属元素的第二位.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com