
| A. | 增大压强和降低温度均可增大气体在水中溶解的体积 | |
| B. | 将KNO3、Ca(OH)2的饱和溶液降温后仍是饱和溶液 | |
| C. | 将食盐、蔗糖溶于水后,溶质均以分子形式存在 | |
| D. | 室温下将1gCaO投入到99g水中所得溶液中溶质的质量分数为1% |
分析 A、利用气体的溶解度随温度的升高而减小,随着压强的增大而增大,进行分析判断.
B、根据KNO3、Ca(OH)2的溶解度受温度影响的变化趋势,进行分析判断.
C、根据食盐、蔗糖的微观构成,进行分析判断.
D、根据氧化钙与水反应生成氢氧化钙,氢氧化钙为溶于水,进行分析判断.
解答 解:A、气体的溶解度随温度的升高而减小,随着压强的增大而增大,增大压强和降低温度均可增大气体在水中溶解的体积,故选项说法正确.
B、KNO3的溶解度随着温度的降低而减小,Ca(OH)2的溶解度随着温度的降低而增大,饱和溶液降温后,氢氧化钙的溶解度增大,溶液变为不饱和溶液,故选项说法错误.
C、食盐是由钠离子和氯离子构成的,溶质以离子形式存在,故选项说法错误.
D、氧化钙与水反应生成氢氧化钙,生成氢氧化钙的质量大于1g,但氢氧化钙微溶于水,常温下氢氧化钙的溶解度为0.17g,则所得饱和溶液中溶质质量分数为$\frac{0.17g}{100g}$×100%<1%,故选项说法错误.
故选:A.
点评 本题难度不大,掌握溶质质量分数的计算方法、气体溶解度的影响因素、常见物质的微观构成等是正确解答本题的关键.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:实验探究题
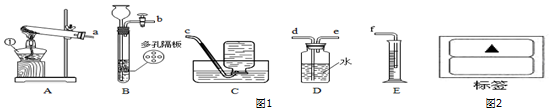
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2个氢分子:2H | B. | 3个氧离子:O${\;}_{3}^{2-}$ | ||
| C. | 氧化铜中铜元素的化合价:$\stackrel{+2}{Cu}O$ | D. | 2个硫酸根离子:2SO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 玉米地的玉米叶子发黄,须及时施加氮肥,如NH4NO3 | |
| B. | 铵态氮肥与氢氧化钙混合时有刺激性气体生成,可使肥效增强 | |
| C. | 过多的营养物质如尿素等进入水体会使水体恶化,出现“水华”现象 | |
| D. | KH2PO4属于复合肥 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
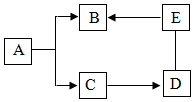 已知A、B、C、D、E是初中化学常见的化合物,其中B、C都是氧化物,D是一种碱,其相对分子质量为74,A、B、D、E属于不同类别的化合物.图中“-”表示相连的物质间能发生反应,“→”表示物质间存在转化关系.
已知A、B、C、D、E是初中化学常见的化合物,其中B、C都是氧化物,D是一种碱,其相对分子质量为74,A、B、D、E属于不同类别的化合物.图中“-”表示相连的物质间能发生反应,“→”表示物质间存在转化关系.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com