
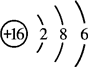 硫(S)元素的原子结构示意图为.该元素的原子核外有
硫(S)元素的原子结构示意图为.该元素的原子核外有

科目:初中化学 来源: 题型:阅读理解
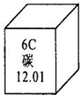 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.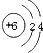
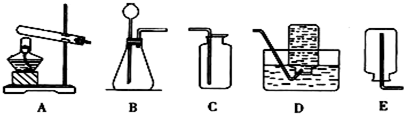
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 1 | 1H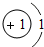 |
2He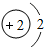 | ||||||
| 2 | 3Li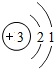 |
4Be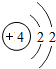 |
5B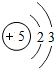 |
6C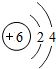 |
7N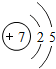 |
8O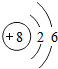 |
9F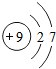 |
10Ne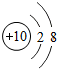 |
| 3 | 11Na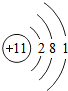 |
12Mg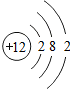 |
13Al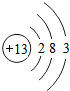 |
14Si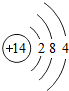 |
15P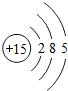 |
16S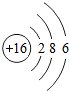 |
17Cl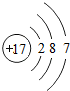 |
18Ar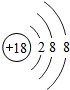 |
查看答案和解析>>
科目:初中化学 来源: 题型:
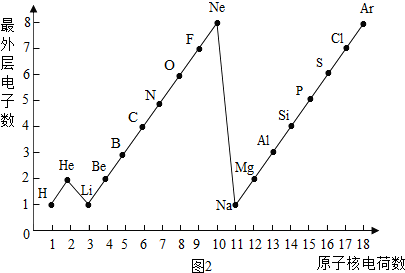
下图是元素周期表中1—18号元素的原子结构示
意图,观察下图,探究下列问题:


(1)核外电子是 排布的。第一层电子数不超过 个;第二层电子数不超过 个;最外层电子数不超过 个。
(2)周期数== 。同一周期的元素,① 相同;
② 逐渐递增;③每周期开头的是 类型的元素,靠近尾部的是 类型的元素,结尾的是 类型的元素。
(3)族数== 。同族元素,① 相同;
② 相似;③ 逐渐递增。
(4)填充下表:
| 元素种类 | 举 例 | 原子的最外层电子数 | 得失电子的趋势 | 元素的化学性质 |
| ①金属元素 | Na、Mg、Al | |||
| ②非金属元素 | O、Cl、S、P | |||
| ③稀有气体元素 | He、Ne、Ar |
(5)最外层为 个电子(只有1个电子层时 个)的结构称为稳定结构。在化学反应中,元素的原子通过得或失电子形成相对稳定结构。
结论:元素的化学性质与 ,特别是 有密切的关系。即 决定元素的化学性质。
查看答案和解析>>
科目:初中化学 来源:2012-2013学年广东省清远市太和镇回澜中学九年级(上)第一次月考化学试卷(解析版) 题型:填空题
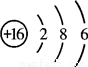
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com