
���� ��1�����ݽ��ʯ��ʯī��C60�Ľṹ�����ʾ��������
��2�����ݴ����ƵĻ�ѧʽ����Ԫ�������ȣ����ݼ�����ȼ�����ɶ�����̼��ˮ��д��ѧ����ʽ��
��3��һ����̼����������Ӧ��ԭ���Լ�ע�������Ϥ�������ʵļ��飻
��4�����ݴ�����̼��Ƶ�������϶�Ӧ�Ļ�ѧ����ʽ�����������Ȼ��Ƶ������Ͷ�����̼�����������������Ӧ��Һ������������
��� �⣺
��1��
A�����ʯ��ʯī��C60����̼Ԫ�صĵ��ʣ���������ͬһ���ʣ�����
B�����ʯ��ʯī��C60����̼Ԫ�صĵ��ʣ������������ǵ�ԭ�����з�ʽ��ͬ�����Ժܶ����ʲ�ͬ����ȷ��
C�����ʯ��ʯī��C60 �У�ֻ��ʯī�ܵ��磬����
D�����ʯ��ʯī��C60����̼Ԫ�صĵ��ʣ�̼�ڳ������ȶ������Գ��������Ƕ�������������Ӧ������
��ѡ��B��
��2��
����ˮ�����ƣ�CH3COONa����C��O����Ԫ�ص�������Ϊ��12��2������16��2��=3��4��
�ڼ�����ȫȼ���Ǽ���������ڵ�ȼ�����������ɶ�����̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��CH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O��
��3��
��CO��Fe2O3��Ӧ�ڸ��µ�������������Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ 3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
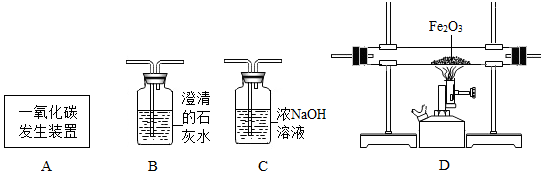
����Ŀ�����Ҫ��Ϊ��������ͼװ�ÿ���CO��ԭFe2O3��ʵ�飬������÷�Ӧ���ɵ���������������Ϊ����֪��A ��ȡ��CO�����л���������CO2�����Լ����ơ�װ�ò����ظ�ʹ�á��������趨��ǰ����ÿһ��������ȫ��Ӧ�������յģ������������ƣ�Ҫ�ȳ�ȥ���е����ʶ�����̼���������Ӱ�쵽���ɵĶ�����̼�ĸ��ţ���������ͨ��װ�õ�˳����A��C����ȥһ����̼�л��еĶ�����̼������Ӱ���������ɵĶ�����̼�ļ��飩��D��һ����̼��ԭ����������B�����������˶�����̼���������������װ�ò����ظ�ʹ�ã��������A��C�����ն�����̼����B�����������̼���ճ��ף���D��B����
�����ڹ����п���ʣ���ж���һ����̼������Ӧ�ü���β��������
��4��̼���80%��ʯ��ʯ12.5g���е�̼��Ƶ�����Ϊ12.5g��80%=10g
�����ɵ��Ȼ��Ƶ�����Ϊx�����ɵĶ�����̼������Ϊy
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 111 44
10g x y
$\frac{100}{10g}$=$\frac{111}{x}$=$\frac{44}{y}$
x=11.1g
y=4.4g
��ǡ����ȫ��Ӧ��������Һ�����ʵ���������Ϊ��$\frac{11.1g}{10g+94.4g-4.4g}$��100%=11.1%
�ʴ�Ϊ��
��1��B��
��2��
��3��4��
��CH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O��
��3��
��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��C��D��B��
�ۼ�β��������
��4��11.1%
���� ���ݻ�ѧ����ʽ����ʱ����һҪ��ȷ��д��ѧ����ʽ���ڶ�Ҫʹ����ȷ�����ݣ������������Ҫ������


 ȫ��������ϵ�д�
ȫ��������ϵ�д� һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | �������� | ��ȥ���ʵķ��� |
| A | CO2 | CO | �������ȼ |
| B | CaO���� | CaCO3 | �ܽ⣬���ˣ��������ᾧ |
| C | Cu��NO3��2��Һ | AgNO3 | �������ͭ�ۣ���ַ�Ӧ����� |
| D | NaCl��Һ | Na2CO3 | ����������ϡ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ӫ���ɷ� | ˮ�� | ������ | ֬�� | ���� | X | �ơ��ס�����п |
| ���� | 92.5g | 0.7g | 0.2g | 6.1g | 6.8mg | 17.1mg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NO | B�� | NO2 | C�� | N2 | D�� | N2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com