
| 物质 | 杂质 | 试剂 | |
| A | CO2 | HCl气体 | NaOH溶液 |
| B | NaCl溶液 | Na2CO3 | 适量稀硫酸 |
| C | NaOH溶液 | Ca(OH)2 | 过量纯碱溶液 |
| D | CaCO3 | Na2CO3 | 水 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的试剂错误.
B、Na2CO3能与适量稀硫酸反应生成硫酸钠、水和二氧化碳,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项所采取的试剂错误.
C、Ca(OH)2能与过量纯碱溶液反应生成碳酸钙沉淀和氢氧化钠,能除去杂质但引入了新的杂质纯碱(过量的),不符合除杂原则,故选项所采取的试剂错误.
D、Na2CO3易溶于水,CaCO3难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的试剂正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:选择题
| 现象或事实 | 解释 | |
| A | 墙内开花墙外香 | 分子在不停地远动 |
| B | H2O2能杀菌消毒,而H2O不能 | 分子的构成不同 |
| C | 1个水分子质量约为3×10-26kg | 分子很小 |
| D | 物体热胀冷缩 | 温度变化,分子可变大可变小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素是一种有机高分子化合物 | |
| B. | 青蒿素中碳、氧元素个数比为3:1 | |
| C. | 青蒿素中氢元素的质量分数最小 | |
| D. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 液体 | 血浆 | 乳汁 | 唾液 | 胆汁 | 胰液 | 胃液 |
| pH范围 | 7.35-7.45 | 6.6-7.6 | 6.6-7.1 | 7.1-7.3 | 7.5-8.0 | 0.9-1.5 |
| A. | 血浆 | B. | 乳汁 | C. | 唾液 | D. | 胃液 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
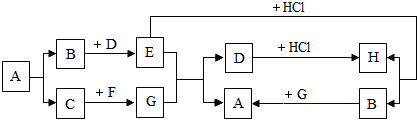
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com