
右图为某学习小组在白色点滴板上进行的有关“碱的化学性质”的探究实验。
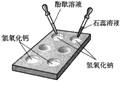
(1)使用白色点滴板进行实验的优点是 (答一点);
(2)氢氧化钠溶液和氢氧化钙溶液都能使无色的酚酞试液变红,是因为
在不同碱的溶液中都含有相同的 离子。
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:初中化学 来源: 题型:
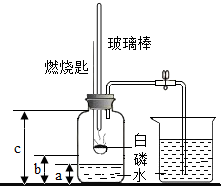 某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.
某化学研究性学习小组在学习了“空气中氧气含量测定”实验的基础上,改进了教材中的实验,设计出如图所示的实验装置.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
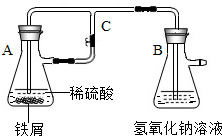 某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:| 资料名称 | 物理性质描述 | 化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3.这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+. |
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
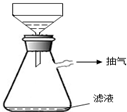 硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录:
硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录:
| ||
| ||
| Al片(未打磨) | Al片(打磨) | |
| CuSO4溶液 (5%,5mL) |
无变化,数小时后铝片上附有极少气泡,几乎无红色物质 | 极少气泡,附着极少红色物质,持续较长时间 |
| CuSO4溶液 (10%,5mL) |
无变化,数小时后铝片附有稍多气泡,仅有极少红色斑点 | 稍多气泡,附着极少(多于5%)红色物质,持续较长时间 |
| CuCl2溶液 (5%,5mL) |
多量气泡,迅速出现红色物质,很快溶液变成无色,且温度升高 | 更多量气泡,迅速出现红色物质,很快溶液变成无色,且温度升高 |
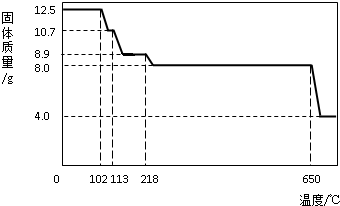
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2008年浙江省温州市苍南县初中知识竞赛科学试卷(化学部分)(解析版) 题型:解答题
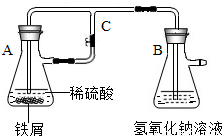 某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:| 资料名称 | 物理性质描述 | 化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3.这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+. |
 Fe(OH)2+nH2O.
Fe(OH)2+nH2O.查看答案和解析>>
科目:初中化学 来源:2011-2012学年北京市东城区普通校联考九年级(上)期中化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com