
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(2)熟记常见仪器的名称;
(3)根据天平的使用注意事项来考虑;
(4)根据图示可知操作步骤;
(5)根据溶质质量分数的计算公式考虑溶质质量分数的偏大偏小情况,根据量筒的选取方法推出选取量筒的量程.
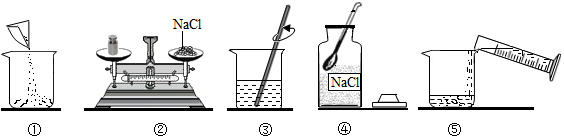
解答 解:(1)100g溶质质量分数为12.5%的NaCl溶液的步骤:计算、称量(量取)、溶解、装瓶贴签,用图示的序号表示为:④②①⑤③.
(2)通过分析可知,配制过程中使用的四种玻璃仪器,分别是广口瓶、玻璃棒、烧杯、量筒;
(3)托盘天平使用前校零,使用时左物右码,m(物体)=m(砝码)+m(游码).图②中是左盘砝码右盘游码,此时
m(砝码)=m(物体)+m(游码),所称药品质量小于实际所需质量.
(4)根据图示很明显看出溶解的步骤;
(5)溶质的质量=溶液的质量×溶质的质量分数=100g×12.5%=12.5g,氯化钠中含杂质,溶质的量变少,故质量分数偏小.溶剂水的质量为100g-12.5g=87.5g,通过密度可求算出水的体积为87.5mL,选择的100mL的量筒.
故答案为:(1)④②①⑤③(2)玻璃棒、烧杯;(3)②;所得溶液质量分数偏小;(4)溶解;(5)12.5; 偏小; ③.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器与作用等是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 氧气约占空气体积的$\frac{1}{5}$ | |
| B. | 氧气能助燃 | |
| C. | 氧气是一种可燃性气体 | |
| D. | 氧气是一种化学性质比较活泼的非金属单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用过滤法将硫酸钠溶液与氯化钡溶液混合后生成的硫酸钡分离出来 | |
| B. | 用蒸发的方法可以除去酒精中的水分 | |
| C. | 用过滤的方法可以除去NaOH溶液中的Ba(OH)2 | |
| D. | 用蒸发的方法从含有少量氯化钠的硝酸钾样品中得到硝酸钾晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com