
���� ��1���ɸ������ʵ��ܽ�ȷ�����
��2�����ݺ��е�Ԫ�صĻ������ڵ��ʽ��
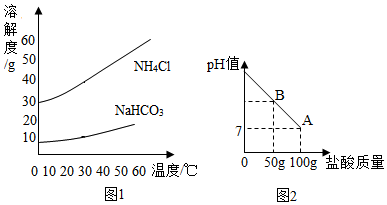
��3������ͼʾ��֪������������ϡ������ͼ��B��ʱ����Һ�����ԣ��ձ�����Һ�������Ϊ�Ȼ��ƺ��Ȼ�����
����̼������ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����ϡ�������Ȼ�����������ɷ�Ӧ�Ļ�ѧ����ʽ����������Ȼ��Ƶ��������μӷ�Ӧ��̼���Ƶ�������
��� �⣺��1������ƴ���������NaHCO3��NH4Cl��������Ϊ84��53.5����NH4Cl�����ܽ�ȱ�NH4ClС������ȴﵽ���ͣ�
��2���Ȼ�刺������������еĵ��ʣ��Ȼ����һ�ֵ��ʣ���ʹС����ҶɫŨ�̣��ٽ�С��������
��3���ٵ���������ϡ������ͼ��B��ʱ����Һ�ʼ��ԣ��ձ�����Һ�������Ϊ�Ȼ��ƺ�̼���ƣ�
ǡ����ȫ��Ӧʱ����ϡ��100g��100gϡ�������Ȼ��������=100g��7.3%=7.3g��
�������Ȼ��Ƶ�����Ϊx���μӷ�Ӧ��̼���Ƶ�����Ϊy�����ɶ�����̼���������Ϊz
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106 73 117 44
y 7.3g x z
$\frac{106}{y}=\frac{73}{7.3g}=\frac{117}{x}=\frac{44}{z}$
y=10.6g
x=11.7g
z=4.4g
����Na2CO3��NaCl�Ļ������Ʒ�У���NaCl������Ϊ13.6g-10.6g=3g��
�۴��¶�ʱ���ò�������Һ������=13.6g+100g-4.4g=109.2g
�𰸣�
��1�����ɵ�NaHCO3������NH4Cl�����ܽ�ȱ�NH4ClС���ȴﵽ���ͣ�
��2������
��3����NaCl��Na2CO3��
��3��
�۴��¶�ʱ���ò�������Һ��������109.2g��
���� �����ѶȱȽϴ��漰��ˮ����������ԭ������ˮɹ�ε�ԭ�������ӵ�ԭ���������Ƽ��ԭ�����������ݣ�Ҫͨ�����������ܽᣮ


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
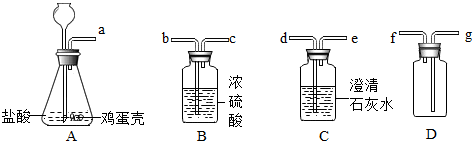
 A��B��C��DΪ���л�ѧ�������������ʣ�����֮������ͼ��ʾ��ת���ͷ�Ӧ��ϵ����������ʾijһ�����ʾ�һ����Ӧ��ת��Ϊ��һ�����ʣ���-����ʾ�����������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ����
A��B��C��DΪ���л�ѧ�������������ʣ�����֮������ͼ��ʾ��ת���ͷ�Ӧ��ϵ����������ʾijһ�����ʾ�һ����Ӧ��ת��Ϊ��һ�����ʣ���-����ʾ�����������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �����õ����� | B�� | �٢ܵĻ�ѧ���ʱȽ����� | ||
| C�� | ����һ�������� | D�� | �٢�����ͬ��Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.6g | B�� | 6.3g | C�� | 8g | D�� | 6.5g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
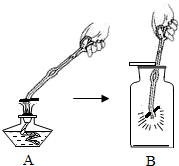 ��ͼ��ʾ���ǡ�ľ̿��������ȼ�ա���һʵ�飬��ش�
��ͼ��ʾ���ǡ�ľ̿��������ȼ�ա���һʵ�飬��ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ۢܢݢ� | C�� | �ڢۢߢ� | D�� | �ۢܢޢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com