
【题目】硼氢化钠【化学式(NaBH4)】,是一种安全车载氢源。
(l)硼氢化钠中Na、B、H元素的质最比为_______(最简整数比);
(2)硼氢化钠中氢元素的化合价为-1价,硼元素的化合价为______。
科目:初中化学 来源: 题型:
【题目】下列有关分子原子的观点正确的是( )
选项 | 事实 | 解释 |
A | 氧分子比氮原子大 | 分子一定比原子大 |
B | 10毫升水和10毫升水混合,无明显变化 | 分子之间没有间隔 |
C | 水电解是化学变化 | 水分子本身发生改变,变成其他物质的分子 |
D | 水分子不显电性 | 水分子中没有带电的粒子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a.b、c三种物质的溶解度曲线,下列有关说法不正确的是( )
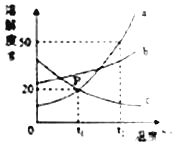
A.P点表示t1℃时a和c的溶解度均为20g
B.t2℃时,溶质质量分数为30%的a溶液是饱和溶液
C.从a和c的混和溶液中提纯a,可采用降温结晶的方法
D.将t1℃时a、b、c的饱和溶液分别升温到t2℃,所得溶液中溶质的质量分数大小顺序为:b>a>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了将混有硫酸钾、氯化钙、碳酸氢铵(不稳定,受热易分解生成氨气、二氧化碳和水)的氯化钾提纯,并制得纯净的氯化钾溶液,某同学设计的实验流程如下:
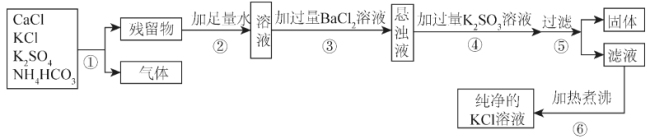
请根据以上流程图中的信息,回答下列问题:
(1)步骤①中除去碳酸氢铵的方法是_____________________________________;
(2)步骤④中加过量碳酸钾溶液的目的是_________________________________;
(3)此设计方案是否严谨?并说明理由___________________________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想:
a.可能是二氧化碳; b.可能是一氧化碳。
并设计如图所示装置进行实验,预期的实验现象及结论如下:
Ⅰ.若澄清的石灰水变浑浊,则气体为二氧化碳;
Ⅱ.若澄清的石灰水不变浑浊,则气体为一氧化碳.
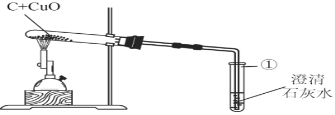
请你分析并回答:
(1)该同学的猜想是否严谨?请你说明理由:_________;___________ ;
(2)设计一个实验,验证⑴中你的理由。请简述你的实验方案____________________________;
(3)该实验装置存在的缺陷是________________________;
(4)反应结束时,停止实验的操作步骤是________________________;
(5)实验后发现试管①内壁上附着不易用试管刷洗净的固体生成物,清洗试管①的方法是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图中甲~戊是初中化学教材中常见物质。甲、戊为氧化物且甲为黑色固体,乙、丙分别是酸和碱中的一种,丁是大理石的主要成分。(图“—”表示相连的物质间可发生反应,“→”表示一种物质可转化为另一种物质,反应条件、部分反应物与生成物均已略去。)下列说法中不正确的是
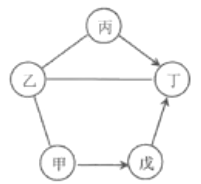
A.乙溶液能使紫色石蕊溶液变红 B.丙溶液能与戊反应生成丁
C.甲→戊只能通过置换反应实现 D.不能由甲通过一步反应生成丁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
研究主题:水溶液中复分解反应的实质
相关信息:一定体积的溶液中,离子的数目越多,其离子的浓度越大.电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小.相同温度下同种溶液电导率越大,离子浓度越大.
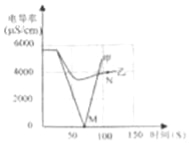
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示.
①写出Ba(OH)2与H2SO4反应的化学方程式 .
②甲曲线M点时混合液体呈 色;
③通过对甲曲线的分析,下列说法错误的是 (填序号).
A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4
B.M点时离子浓度几乎为零 C.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示.
①通过对乙曲线的分析,下列说法错误的是 (填序号).
A.开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B.电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C.整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是 (填离子符号).
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度 (填“增大”或“减小”).
(3)拓展:①请根据示例仿写离子方程式.
示例AgNO3+NaCl=AgCl↓+NaNO3离子方程式:Ag++Cl﹣=AgCl↓
仿写:BaCl2+Na2SO4=BaSO4↓+2NaCl离子方程式: .
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失.请推测此过程的溶液中Ca2+的浓度变化情况 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com