
 (1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝.金属大规模被使用的先后顺序跟(选填字母)______(A.地壳中金属元素的含量 B.金属的导电性 C.金属的活动性)关系最大;目前世界上已有50%以上的废钢铁得到回收利用,其目的是______(A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈);生锈的铁制品放入盛有过量稀盐酸的洗槽中,观察到溶液变黄,有无色气泡逸出.写出其中一个反应的化学方程式______,其反应类型是______.若要验证银、铁、锌的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是______、______.
(1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝.金属大规模被使用的先后顺序跟(选填字母)______(A.地壳中金属元素的含量 B.金属的导电性 C.金属的活动性)关系最大;目前世界上已有50%以上的废钢铁得到回收利用,其目的是______(A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈);生锈的铁制品放入盛有过量稀盐酸的洗槽中,观察到溶液变黄,有无色气泡逸出.写出其中一个反应的化学方程式______,其反应类型是______.若要验证银、铁、锌的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是______、______.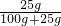 ×100%=20%;
×100%=20%;

 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
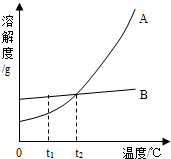 (2012?宿迁)(1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝.金属大规模被使用的先后顺序跟(选填字母)
(2012?宿迁)(1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝.金属大规模被使用的先后顺序跟(选填字母)查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
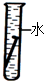 B、
B、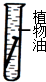 C、
C、 D、
D、
| 金属 | 铁 | 锰 |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 |
| 结论 | 活动性铁 < < (填“>”“<”)锰 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com