
| 气体 性质 | H2 | CO2 | O2 | N2 | Cl2 |
| 气体的沸点/℃ | -252 | -78 | -183 | -196 | -34 |
| 被吸附体积/mL | 4.5 | 97 | 35 | 11 | 494 |
分析 由表中数据分析:不是每个气体分子所含原子个数越多,越容易被吸附,比较CO2和Cl2的表中相关数据既得结果;不是沸点越低的气体,越易被吸附,比较O2和N2表中相关数据既得结果;气体是化合物时,易被吸附,此说法也不正确,比较CO2和Cl2的表中相关数据既得结果;气体的相对分子质量越大,越易被吸附,此说法符合表中相关数据,可比较表中五种气体的数据即可.
解答 解:①不是每个气体分子所含原子个数越多,越容易被吸附,比较CO2和Cl2的表中相关数据既得结果;故错误;
②沸点越高的气体,越易被吸附,此说法符合表中相关数据,可比较表中五种气体的数据即可;故正确;
③气体是化合物时,易被吸附,此说法也不正确,比较CO2和Cl2的表中相关数据既得结果;故错误;
④气体的相对分子质量越大,越易被吸附,此说法符合表中相关数据,可比较表中五种气体的数据即可.故正确;
经以上分析可知,气体的相对分子质量和沸点决定着气体被吸附剂吸附的多少;相对分子质量越大,沸点越高的气体容易被吸附剂吸附.
故填:②④.
点评 本题主要分析了气体的分子组成、沸点、相对分子质量等与吸附剂吸附能力之间的关系.分析时以表格内数据为依据进行一一比较即得结果.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
| 温度(℃) | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| 氯化钠(克) | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 温度(℃) | 0 | 10 | 20 | 30 | … | 90 | |
| 纯碱(克) | 7.1 | 12.5 | 21.5 | 38.8 | … | 43.9 | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 20 | 30 | 40 | 50 |
| KCl | 34.0g | 37.0g | 40.0g | 42.6g |
| KNO3 | 31.6g | 45.8g | 63.9g | 85.5g |
| A. | 20℃时KCl溶解度大于KNO3的溶解度 | |
| B. | 两物质的溶解度相等的温度在20℃-30℃间 | |
| C. | 在40℃时,10g水中加入5gKCl可得到33.3%的KCl溶液 | |
| D. | 在50℃时,10g KNO3中加入20克水,充分溶解后再降温到30℃,有KNO3固体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
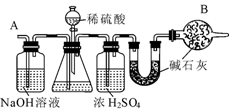
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH<7 (填“>”、“=”或“<”) | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 上浮 | B. | 悬浮 | C. | 下沉 | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com