
下列选项中物质的名称、俗称、化学式一致的是 ( )
A. 碳酸钠 小苏打 Na2CO3 B. 氢氧化钠 纯碱 NaOH
C. 二氧化碳 干冰 CO2 D. 氢氧化钙 石灰石 Ca(OH)2
C 【解析】A、碳酸钠是苏打,不是小苏打,错误; B、纯碱是碳酸钠,不是氢氧化钠,错误; C、固态二氧化碳是干冰,正确; D、石灰石是碳酸钙,不是氢氧化钙,错误。故选C。科目:初中化学 来源:安徽省2017-2018学年九年级下学期4月段考化学试卷 题型:实验题
研究性学习在实验室进行了化学实验,向一盛有镁和铜混合物的烧杯中加入一定量的稀盐酸,充分反应后,观察到烧杯中有固体剩余,对反应后所得溶液中溶质的成分进行探究.
(1)写出上述烧杯中发生反应的化学方程式 .
(2)对反应后所得溶液中溶质的成分进行猜想,请你再补充一种猜想.
【猜想】小光猜想:溶质为氯化镁;
小红猜想:溶质为氯化铜和氯化镁;
你的猜想:溶质为 .
(3)【讨论】你认为 的猜想不合理,理由是 .
(4)【实验】若你的猜想正确,设计一种实验方案证明你的猜想并完成下表:
实验步骤 | 实验现象 | 实验结论 |
取少量反应后溶液: |
| 你的猜想正确 |
(5)【应用】如果你的猜想正确,把该废液倒入铁质下水管道可能造成的一条危害 .
(1)2HCl+Mg═MgCl2+H2↑;(2)氯化镁和氯化氢; (3)小红;由于活动性由于铜在H后面,所以铜不能与盐酸反应,所以溶质中不可能有氯化铜; (4) 实验步骤 实验现象 实验结论 取少量反应后溶液:滴加几滴石蕊试液 溶液变红色 你的猜想正确 (5)腐蚀下水道. 【解析】(1)镁与盐酸反应生成...查看答案和解析>>
科目:初中化学 来源:江苏省无锡市滨湖区2018届九年级第一次模拟考试化学试卷 题型:单选题
有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按照下列流程进行实验。
下列说法正确的是
A. 滤渣a是CaCO3
B. 白色沉淀b中可能含有MgCO3
C. 滤液中一定存在的溶质是NaCl、BaCl2、NaOH
D. 该白色固体样品中一定含有CaCO3、BaCl2、NaOH、MgCl2,可能含有Na2SO4
C 【解析】A、样品溶于水得到滤渣1.5g,能够全部溶于稀盐酸,且产生0.44g的二氧化碳,说明沉淀一定含有碳酸钙,一定没有硫酸钡; 设产生0.44g的二氧化碳需要碳酸钙的质量为x. CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 44 x...查看答案和解析>>
科目:初中化学 来源:甘肃省2018届九年级第一次模拟考试化学试卷 题型:实验题
下图是化学实验中常用的几种装置。请回答下列问题:



(1)指出有编号的仪器名称:①__________,②________。
(2)写出实验室利用上述A装置制取氧气的化学反应方程式___________________________。
(3)若用F装置干燥生成的氧气,F中盛放的液体试剂是_________,气体应从__________端导入(填“a”或“b”)。
(4)用KClO3制氧气时需加MnO2作催化剂。若在KClO3中加少量的KMnO4,也能加快KCIO3的分解。用文字说明其原因_____________________。
(5)实验室要制取二氧化碳,写出反应的化学方程式___________________________________,
使用G装置制取比B装置的突出优点是___________________,收集CO2的装置是________,(填代号),验满的方法是_________________________________。
酒精灯 长颈漏斗 2KMnO? = K₂MnO? +MnO₂ +O₂↑ 浓硫酸 a 高锰酸钾分解产生了二氧化锰 CaCO3+2HCl==CaCl2+H2O+CO2↑ 控制化学反应的速率 D 燃着的木条放在集气瓶口,熄灭则满 【解析】(1)仪器①是酒精灯,仪器②是长颈漏斗;(2) (2)A装置是用高锰酸钾加热分解生成锰酸钾和二氧化锰和氧气,反应方程式为2KMnO? = K₂MnO? +M...查看答案和解析>>
科目:初中化学 来源:甘肃省2018届九年级第一次模拟考试化学试卷 题型:单选题
煤气中加入有特殊气味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生的反应为:2X+9O2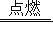 4CO2+2SO2+6H2O,则X是( )
4CO2+2SO2+6H2O,则X是( )
A.C4H12S2 B.C2H6S C.C2H6O2 D.C2H6
B 【解析】【解析】 反应后生成物4CO2、2SO2、6H2O中,共有4个碳原子、2个硫原子、18个氧原子、12个氢原子,根据质量守恒定律,反应前物质中原子的种类和数目不变,所以2X+9O2中已有18个氧原子,2X中应含有4个碳原子、2个硫原子、12个氢原子,则X的组成为2个碳原子、1个硫原子、6个氢原子, 故选:B.查看答案和解析>>
科目:初中化学 来源:湖北省宜昌市东部2018届九年级下学期期中考试化学试卷 题型:填空题
某废液中可能含有盐酸、氯化钠、硫酸钠、碳酸钠、硝酸钾中的一种或几种。为了检验废液的成分,

小鹏同学的探究过程如下:
⑴原废液中一定含有的溶质是_______________(用化学符号填空,下同);可能含有的溶质是__________。
⑵步骤④发生反应的化学方程式为_________________;
⑶将步骤②的“足量”改为“少量”,不能证明________________的存在;
⑷溶液D中一定含有的阳离子有__________________;反思:检验物质的成分应注意排除干扰因素。
【答案】 Na2SO4、Na2CO3、NaCl KNO3 2HNO3+BaCO3=Ba(NO3)2+H2O+CO2↑ 碳酸钠 钠离子
【解析】(1)加入锌粒无明显现象,说明溶液中没有稀盐酸,加入硝酸钡后后白色沉淀生成,白色的沉淀加入稀硝酸后沉淀部分溶解,说明溶液中一定有碳酸钠和硫酸钠, 溶液B中加入硝酸银有白色沉淀生成,说明B中一定有氯化钠,故原溶液中一定与的物质是Na2SO4、Na2CO3、NaCl;可能含有KNO3;
(2)步骤4 是硝酸与碳酸钡反应生成硝酸钡和二氧化碳和水,反应方程式为2HNO3 + BaCO3 = Ba(NO3)2 + H2O + CO2↑
(3)将步骤②的“足量”改为“少量”,不能证明碳酸钠的存在;溶液中一定存在的是硝酸钠,故阳离子是钠离子;
【题型】流程题
【结束】
28
某班学生分三组分别做了二氧化碳制取和性质验证实验,如下图所示。

甲 乙 丙
实验结束后,老师取两份等质量的丙废液,分别与甲、乙废液混合。将甲废液与丙废液倒入烧杯A中,有白色沉淀生成;将乙废液与丙废液倒入烧杯B中,有气泡产生。
请填空:
(1)甲废液与乙废液所含溶质的成分可能不同的是 (用化学式填空,下同)。
(2)烧杯A中沉淀的成分一定有 。
(3)另取少量丙废液样品,加入足量的氯化钡溶液,有白色沉淀生成。过滤,向滤液中滴加氯化铁溶液,观察到有红褐色沉淀生成,未发现其他明显现象。
由此推测出,丙废液溶质的成分是 ,丙废液与氯化钡溶液反应的化学方程式为 ,烧杯A的上层清液中溶质的成分一定有 。
(1)HCl (2)CaCO3 (3)Na2CO3、NaOH;BaCl2+Na2CO3=BaCO3↓+2NaCl;NaCl、NaOH 【解析】 试题分析:(1)丙中的氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠与稀盐酸反应生成二氧化碳气体、与氯化钙溶液反应生成碳酸钙白色沉淀,大理石与稀盐酸反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑ ; 甲、乙废液中都有溶质...查看答案和解析>>
科目:初中化学 来源:湖北省宜昌市东部2018届九年级下学期期中考试化学试卷 题型:填空题
t1℃时,将等质量的硝酸钾和氯化钾分配加入到各盛有10g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.

(1)烧杯①中溶解的溶质是______(写名称或化学式);
(2)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水____g;
(3)关于图1中烧杯内的物质,下列说法正确的是____________.
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
KCl 50g A D 【解析】(1)在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。由图可知,t1℃时,硝酸钾的溶解度比氯化钾的小,烧杯①中溶解的溶质是氯化钾;(2)饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100%,溶液的稀释过程中溶质的质量不变,将t1℃时,设50g硝酸钾的饱和溶液稀释成10%的溶液,需要水的...查看答案和解析>>
科目:初中化学 来源:湖北省宜昌市东部2018届九年级下学期期中考试化学试卷 题型:单选题
某纯净物X在空气中完全燃烧,反应的化学方程式为:X+2O2 CO2+2H2O,下列关于X的说法正确的是( )
CO2+2H2O,下列关于X的说法正确的是( )
A. X由碳、氢、氧三种元素组成 B. X的相对分子质量为10
C. X中碳、氢元素的质量比为1:4 D. X属于有机化合物
D 【解析】据质量守恒定律可知,化学反应前后原子的种类、个数不变,反应前有4个氧原子,反应后有1个碳原子、 4个氢原子、4个氧原子,所以一个X的分子中有1个碳原子、4个氢原子;X的化学式为CH4,由碳、氢两种元素组成;相对分子质量为12+4=16;碳、氢元素的质量比为12:4=1:3;除一氧化碳、二氧化碳、碳酸、碳酸盐以外的含碳化合物称为有机物。甲烷是最简单的有机物。选D查看答案和解析>>
科目:初中化学 来源:江苏省扬州市高邮2018届九年级下学期一模考试化学试卷 题型:单选题
邮城八景之一的“杨柳堤岸“在春暖花开的时节会柳絮飞扬。为减少柳絮,园林工人将赤霉酸(C19H22O6),注入柳树。关于赤霉酸的说法正确的是
A. 赤霉酸由47个原子构成 B. 氢、氧元素质量比11∶3
C. 氢元素的质量分数最大 D. 相对分子质量为346
D 【解析】A、由赤霉酸的化学式可知,一个赤霉酸分子,由47个原子构成,错误;B、氢、氧元素质量比为(1×22):(16×6)=11∶48,错误;C、碳、氢、氧元素质量比为(12×19):(1×22):(16×6)=114:11∶48,错误;D、相对分子质量为(12×19)+(1×22)+(16×6)=346,正确。故选D。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com