
分析 根据活动性强的金属可以把活动性弱的金属从其盐溶液中置换出来,所以铁可以置换出铜与银但不能置换出铝,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,此现象说明Fe过量没有反应完,所以原混合溶液中的Cu(NO3)2、AgNO3全部被置换生成Cu、Ag和Fe(NO3)2溶液,A1(NO3)3不反应进行分析.
解答 解:混合溶液中的Cu(NO3)2、AgNO3与铁发生置换反应,得到Cu、Ag,铁粉过量,所以滤出固体中含Fe;反应后的溶液中即滤液不再含的Cu(NO3)2、AgNO3,而是含有生成的Fe(NO3)2;由于Al(NO3)3不与Fe发生反应,所以滤液中还含有Al(NO3)3.
故答案为:Al3+ 和Fe2+.
点评 本题是对金属活动性顺序的考查,解题的关键是掌握金属活动性顺序表的意义,只有这样才能做出正确的判断.


科目:初中化学 来源: 题型:解答题
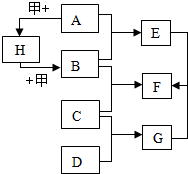 已知A-H为初中常见物质,A为红棕色,是赤铁矿的主要成分,F为紫红色金属,甲是黑色固体,它们相互转化关系如图所示(反应条件、和部分产物已略去).请按要求回答下列问题:
已知A-H为初中常见物质,A为红棕色,是赤铁矿的主要成分,F为紫红色金属,甲是黑色固体,它们相互转化关系如图所示(反应条件、和部分产物已略去).请按要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
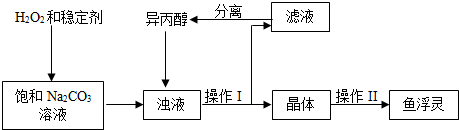

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质名称 | 物质的组成(用化学式表示) | 构成物质的微粒(用符号表示) |
| 干冰 | ||
| 锌 | ||
| 食盐水 | ---------- |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com