
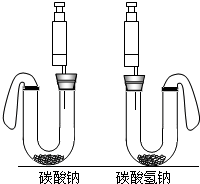
 泡沫灭火器中应用
泡沫灭火器中应用
| ||
| 106 |
| 44 |
| 1g |
| x |
| 44 |
| 106 |
| 84 |
| 44 |
| 1g |
| y |
| 44 |
| 84 |
| 44 |
| 106 |
| 44 |
| 84 |
| ||
| 168 |
| 62 |
| x |
| 3.1g |
| 1.6g |
| 10g |


科目:初中化学 来源: 题型:
| A、活性炭可除去冰箱中的异味 |
| B、干冰用作人工降雨 |
| C、氮气用作焊接金属的保护气 |
| D、稀有气体通电能发出不同颜色的光 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
| 实验内容 | 预计现象 | 预计结论 |
| 将打磨过和没打磨的大小性状相同的锌片置于试管中,加入体积、质量分数相同的盐酸溶液静置 | 打磨过的锌片在相同时间收集的气体更多 | |
| 将打磨过的大小性状相同的锌片置于试管中,加入体积相同10%、20%的盐酸溶液,静置 | 加入20%盐酸的试管在相同时间收集的气体更多 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.
同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | ①有白色沉淀,溶液呈红色. | |
| ② | 小刚的猜想正确. | |
| ③无白色沉淀,溶液呈红色. |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com