
| A. | 插入燃着的木条 | B. | 观察气体颜色 | C. | 闻气体的气味 | D. | 倒入澄清石灰水 |
分析 鉴别空气、氧气、二氧化碳三瓶气体,要求根据三种气体性质的不同,设计的方案能出现三种明显不同的实验现象,才能达到达到一次鉴别出三瓶气体的目的.
解答 解:A、把燃着的木条分别伸入三个集气瓶中,若木条熄灭,则是二氧化碳;若木条燃烧更旺,则是氧气;若木条正常燃烧,则是空气;现象明显,能一次鉴别出这三瓶气体,故选项正确.
B、空气、氧气和二氧化碳三瓶气体均没有颜色、没有气味的气体,用观察气体的颜色的方法无法鉴别,故选项错误.
C、空气、氧气和二氧化碳三瓶气体均没有颜色、没有气味的气体,用闻它们的气味无法鉴别,故选项错误.
D、二氧化碳能使澄清的石灰水变浑浊,用澄清的石灰水只能鉴别出二氧化碳,无法鉴别空气、氧气,故选项错误.
故选:A.
点评 本题考查了常见气体的鉴别方法,解题的关键是利用所要鉴别气体的性质的差别,根据实验中是否出现明显的不同现象判断能否鉴别.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 常温下铝表面氧化膜的生成:Al+O2=Al2O3 | |
| B. | 铜与稀盐酸反应:Cu+2HCl=CuCl2+H2↑ | |
| C. | 甲烷(CH4)燃烧:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | |
| D. | 铁和硫酸铜反应:2Fe+3CuSO4=Fe2(SO4)3+3Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 成分 | 蛋白质 | 油脂 | 糖类 | 钙 | 铁 | 维生素 |
| 质量分数/% | 1.8 | 0.7 | 1.1 | 0.01 | 0.0005 | 0.015 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
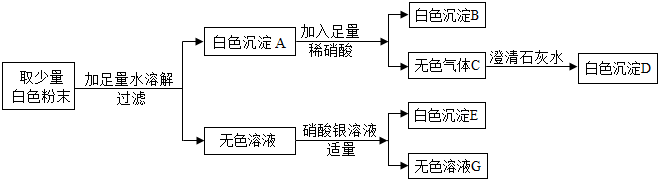
| A. | 无色溶液F中只有NaCl | |
| B. | 沉淀B的化学式为BaSO4 | |
| C. | 原混合物中一定不含CuSO4 | |
| D. | 原混合物中一定含有BaCl2、Na2SO4、Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com