
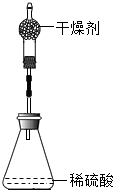
 £Ø2013?ĻĆĆÅ£©ĪŖ²ā¶ØŠæĶŗĻ½šÖŠŠæµÄŗ¬Įæ£¬Č”øĆŗĻ½š·ÅČėČēĶ¼ Ź¢ÓŠĻ”ĮņĖįµÄ׶ŠĪĘæÖŠ£¬·¢Éś·“Ó¦£ŗZn+H2SO4=ZnSO4+H2”ü£®¶ą“ĪŹµŃéŗó£¬Č”Ę½¾łÖµĖłµĆŹż¾ŻČēĻĀ±ķ£ŗ
£Ø2013?ĻĆĆÅ£©ĪŖ²ā¶ØŠæĶŗĻ½šÖŠŠæµÄŗ¬Įæ£¬Č”øĆŗĻ½š·ÅČėČēĶ¼ Ź¢ÓŠĻ”ĮņĖįµÄ׶ŠĪĘæÖŠ£¬·¢Éś·“Ó¦£ŗZn+H2SO4=ZnSO4+H2”ü£®¶ą“ĪŹµŃéŗó£¬Č”Ę½¾łÖµĖłµĆŹż¾ŻČēĻĀ±ķ£ŗ| ·“Ó¦Ē° | ³ä·Ö·“Ó¦ŗó×°ÖĆ¼°·“Ó¦Ź£ÓąĪļÖŹÖŹĮæ | |
| ×°ÖĆŗĶ×ćĮæµÄĻ”ĮņĖįÖŹĮæ | ŠæĶŗĻ½šÖŹĮæ | |
| 342.10g | 16.00g | 357.70g |
| 65 |
| 16.00g”Įx |
| 2 |
| 0.4g |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| ||
| ||
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £Ø2013?ĻĆĆÅ£©¼øÖÖ³£¼ūĪļÖŹÖ®¼äµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ ĖłŹ¾£Øø÷×ÖÄø“ś±ķŅ»ÖÖĪļÖŹ£¬²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļ¼°·“Ó¦Ģõ¼žĀŌČ„£©£®¼ŗÖŖ£ŗ¢ŁĪåÖÖĪļÖŹ¾łŗ¬ĶŌŖĖŲ£¬ĒŅ»ÆŗĻĪļÖŠĶŌŖĖŲµÄ»ÆŗĻ¼Ū¾łĪŖ+2£» ¢ŚA ĪŖµ„ÖŹ£¬ŌŚæÕĘųÖŠ¼ÓČČŗóÉś³ÉŗŚÉ«ĪļÖŹ B£» ¢ŪX ČÜŅŗÓėĢś·“Ó¦æɵƵ½ A£» ¢ÜX ČÜŅŗÓėĀČ»Æ±µČÜŅŗ·“Ó¦æɵƵ½ D£¬Ķ¬Ź±ÓŠ°×É«³ĮµķÉś³É£» ¢ŻD ČÜŅŗÖŠ¼ÓČėÉŁĮæµÄĒāŃõ»ÆÄĘČÜŅŗµĆµ½ E£®½įŗĻŠÅĻ¢ĶʶĻ£ŗ
£Ø2013?ĻĆĆÅ£©¼øÖÖ³£¼ūĪļÖŹÖ®¼äµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ ĖłŹ¾£Øø÷×ÖÄø“ś±ķŅ»ÖÖĪļÖŹ£¬²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļ¼°·“Ó¦Ģõ¼žĀŌČ„£©£®¼ŗÖŖ£ŗ¢ŁĪåÖÖĪļÖŹ¾łŗ¬ĶŌŖĖŲ£¬ĒŅ»ÆŗĻĪļÖŠĶŌŖĖŲµÄ»ÆŗĻ¼Ū¾łĪŖ+2£» ¢ŚA ĪŖµ„ÖŹ£¬ŌŚæÕĘųÖŠ¼ÓČČŗóÉś³ÉŗŚÉ«ĪļÖŹ B£» ¢ŪX ČÜŅŗÓėĢś·“Ó¦æɵƵ½ A£» ¢ÜX ČÜŅŗÓėĀČ»Æ±µČÜŅŗ·“Ó¦æɵƵ½ D£¬Ķ¬Ź±ÓŠ°×É«³ĮµķÉś³É£» ¢ŻD ČÜŅŗÖŠ¼ÓČėÉŁĮæµÄĒāŃõ»ÆÄĘČÜŅŗµĆµ½ E£®½įŗĻŠÅĻ¢ĶʶĻ£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com