


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:初中化学 来源: 题型:
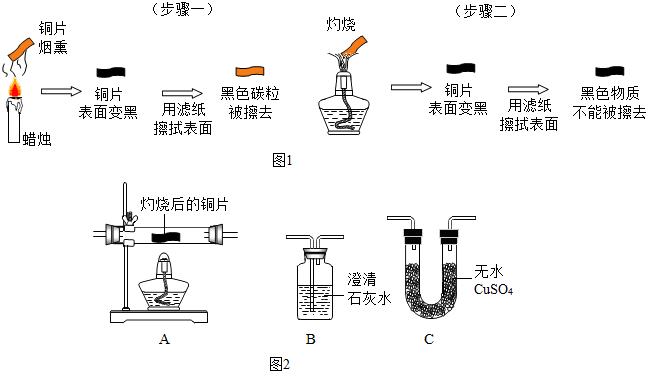
| A、硫在氧气中燃烧,发出淡蓝色火焰,产生刺激性气味的气体 |
| B、红磷在氧气中剧烈燃烧,发出耀眼白光,有大量白色气体生成 |
| C、木炭在氧气中燃烧,发出白光,放出热量伴有使澄清石灰水变浑浊气体 |
| D、铁丝在氧气中剧烈燃烧,火星四射有黑色四氧化三铁固体生成,并放出大量的热 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
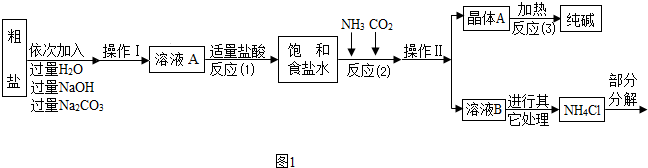
| 选择的装置 | 实验现象 | 实验结论 |
| 样品不含晶体A |

查看答案和解析>>
科目:初中化学 来源: 题型:
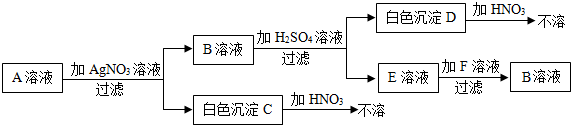
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是某药厂生产的葡萄糖注射液的标签.其溶质葡萄糖的化学式为C6H12O6,是计算:
如图是某药厂生产的葡萄糖注射液的标签.其溶质葡萄糖的化学式为C6H12O6,是计算:查看答案和解析>>
科目:初中化学 来源: 题型:
| 反应次数 | 稀盐酸的质量(g) | 混合物的质量(g) | 产生CO2的质量(g) |
| 1 | 100 | 27.6 | 6.6 |
| 2 | 100 | 36.8 | 8.8 |
| 3 | 100 | 39.0 | 8.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com