
| 次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入锌的质量(g) | 2 | 4 | 6 | 8 | 10 | 12 |
| 稀硫酸的质量(g) | 60 | 60 | 60 | 60 | 60 | 60 |
| 生成的硫酸锌的质量(g) | 5 | 15 | 17 | 17 |
分析 (1)根据生成硫酸锌的质量随加入锌的质量的变化关系得出硫酸锌的质量;
(2)根据实验数据,分析曲线的起点、折点及趋势,绘制出随锌质量增加而生成硫酸锌的质量的关系曲线;
(3)根据表中第四次数据中的硫酸锌质量求出所消耗的锌的质量,然后计算剩余固体质量;
(4)选取硫酸完全反应的第四次实验数据,根据反应的化学方程式,由反应生成的硫酸锌的质量计算出60g硫酸溶液中硫酸的质量,解决硫酸溶液的质量分数.
解答 解:(1)根据第一组实验数据可知,加入2克锌和硫酸反应生成硫酸锌的质量为5克;第二组:加入4克锌和硫酸生成硫酸锌的质量=5克×2═10克;第三组:加入8克锌和硫酸反应应生成硫酸锌的质量=5克×4═20克,但是题目中硫酸锌的质量为17克,所以60克硫酸全部参加反应,锌有剩余,第四组:由于第三组中硫酸已经完全反应,所以硫酸锌的质量不变,即硫酸锌的质量为17克;
(2)设生成17g硫酸锌时,反应掉的锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 161
x 17g
$\frac{65}{161}=\frac{x}{17g}$
x≈7g
(3)第4次实验硫酸完全反应,当第5次实验中金属锌的质量增加时,硫酸已消耗完毕,当硫酸反应完全时反应掉的锌的质量为7g,多余的锌均剩余,若使(10+m)g锌与60g稀硫酸充分反应后,剩余固体质量为(10+m)g-7g=(m+3)g;
(4)设生成17g硫酸锌时消耗硫酸的质量为y
Zn+H2SO4═ZnSO4+H2↑
98 161
y 17g
$\frac{98}{161}=\frac{y}{17g}$
y≈10
稀硫酸的溶质的质量分数为:$\frac{10g}{60g}×100%$≈17%
答:稀硫酸的质量分数为17%.
故答案为:
(1)10,17;
(2)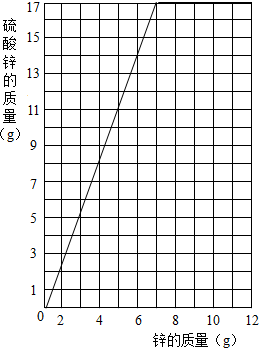 ;
;
(3)3+m;
(4)l7%.
点评 灵活运用数据表中的数据来进行计算,分析表示反应变化特点的曲线时,对于曲线的起点、折点、趋势的分析,可以准确地把握变化的特点.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:初中化学 来源: 题型:选择题
| A. | 用食醋浸泡可除去水壶中的水垢 | |
| B. | 用铜、稀硫酸和空气为原料制取硫酸铜 | |
| C. | 将酚酞试液滴入盐酸和氢氧化钠混合液中,得无色溶液,可证明盐酸过量 | |
| D. | 二氧化碳气体中混有少量杂质氯化氢,将气体通入饱和碳酸氢钠溶液中可除去杂质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | XY、XY2 | B. | X2Y、X2Y3 | C. | XY2、X2Y | D. | XY3、X2Y4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 建在干旱山区可以脱贫致富 | B. | 不宜建在居民区附近 | ||
| C. | 企业有权自主选择基地 | D. | 应建在水源丰富和交通方便的地点 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 代谢产生的 CO2,如不能及时排出,会使血液的 pH 增大 | |
| B. | 无机盐和水虽不能提供能量,却是人体必需的 | |
| C. | 胃液中少量的盐酸可以帮助消化 | |
| D. | 香烟烟气中的 CO 会使血红蛋白携氧能力降低 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 甲、乙、丙三种物质均含地壳中含量最多的元素.甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解成丙;它们之间有如图所示的转化关系(部分物质和反应条件已经略去).则:甲的化学式为H2O2;甲转化成丙的符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;从微观的角度解释甲、乙性质有差异的原因是分子构成不同.
甲、乙、丙三种物质均含地壳中含量最多的元素.甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解成丙;它们之间有如图所示的转化关系(部分物质和反应条件已经略去).则:甲的化学式为H2O2;甲转化成丙的符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;从微观的角度解释甲、乙性质有差异的原因是分子构成不同.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com