
科目:初中化学 来源: 题型:选择题
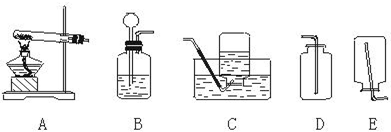
| A. | 胶头滴管:用于吸取和滴加少量液体 | |
| B. | 酒精灯:用外焰给物质加热 | |
| C. | 试管:只能常温时使用 | |
| D. | 玻璃棒:常用于搅拌、过滤或转移物质等 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 1 | 42 | 10 |
| 反应后质量(g) | 4 | 20 | 6 | 待测 |
| A. | 该变化的基本反应类型一定是化合反应 | |
| B. | 丁反应后的质量为13克 | |
| C. | 反应中甲可能是催化剂 | |
| D. | 乙与丙的物质的量之比是19:36 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
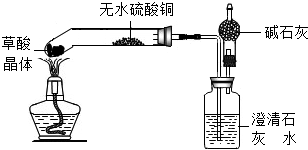 草酸的化学式为H2C2O4,某实验小组对草酸受热分解及其产物进行探究:
草酸的化学式为H2C2O4,某实验小组对草酸受热分解及其产物进行探究:| 实验操作 | 实验现象 | 实验结论 |
| 1.加热草酸晶体 | 无水硫酸铜变蓝色 | 说明有水(H2O)生成. |
| 澄清石灰水变浑浊 | 说明有二氧化碳(CO2)生成. | |
| 2.生成的气体通过碱石灰后,在干燥管的尖嘴处点燃,并在上方罩上内壁附着有澄清石灰水的小烧杯. | 气体燃烧,烧杯内壁的澄清石灰水变浑浊. | 说明有一氧化碳(CO);生成. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| NaHCO3溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾, 将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
| 步骤 | 现象 | 结论与方程式 |
| ①取少量溶于水,加入过量CaCl2溶液. | 产生白色沉淀 | 该反应方程式: CaCl2+Na2CO3═CaCO3↓+2NaCl. |
| ②将上述反应后混合液过滤,取滤液 稀盐酸. | 有气泡冒出 | 证明猜想③成立. |
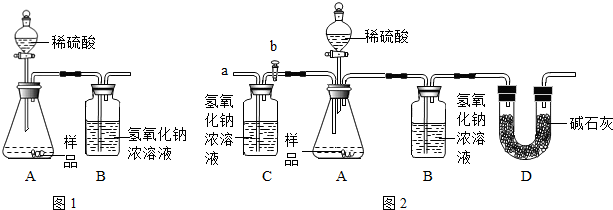
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
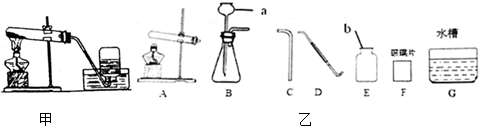
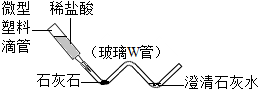
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca5(PO4)3(OH)]的形式存在.牛奶中含钙丰富又易被吸收,且牛奶中的钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签和部分说明.请仔细阅读后回答下列问题.已知羟基磷酸钙的相对分子质量是502.
人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体[Ca5(PO4)3(OH)]的形式存在.牛奶中含钙丰富又易被吸收,且牛奶中的钙和磷比例合适,是健骨的理想食品.如图是某乳业公司纯牛奶包装标签和部分说明.请仔细阅读后回答下列问题.已知羟基磷酸钙的相对分子质量是502.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com