
向部分变质的氢氧化钠溶液中滴加过量稀盐酸,下列图像能正确反映对应变化关系的是( )

科目:初中化学 来源: 题型:
甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如右图所示,下列说法正确的是( )
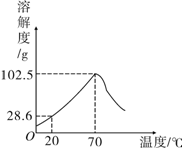
A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100 g甲的饱和溶液中溶质质量为28.6 g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
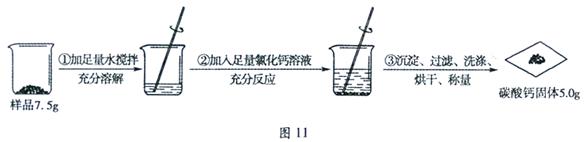
某碳酸钠样品中混有少量氯化钠,根据图11所示信息计算该样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(反应的化学方程式:CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl)
查看答案和解析>>
科目:初中化学 来源: 题型:
要除去下列物质中的少量杂质(括号内物质为杂质),下列实验方案设计中,不合理的是( )
A.NaCl溶液(Na2SO4):加入过量的BaCl2溶液,过滤 B.N2 (O2):将气体缓缓通过灼热的铜网
C.CaCOj (CaCl2):加水溶解一过滤一洗涤一干燥 D.KCl溶液(K2CO3):加入适量的稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种。某化学兴趣小组为探究其成分做了以下实验:
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示;
Ⅱ.取少量B点时的清液于试管中,滴加酚酞溶液,酚酞溶液不变色;
Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示。

请回答下列问题:
(1)BC段可观察到的现象是 , 从C到D液体的pH (填“增大”、“减小”或“不变”);
(2)原白色固体中一定含有 ,可能含有 ;
(3)D点时,溶液中一定含有的溶质是 ;
(4)为进一步探究该白色固体的成分,该组同学取少量原固体样品于试管中,加足量水溶解,加
,过滤;再向滤液中加 ,观察现象。
查看答案和解析>>
科目:初中化学 来源: 题型:
只用石蕊试液就能将下列各组溶液区分开来的是( )
A.NaCl NaOH NaNO3 B.NaOH H2SO4 KNO3
C.HCl NaCl Na2SO4 D.Na2SO4 H2SO4 CuSO4
查看答案和解析>>
科目:初中化学 来源: 题型:
氧化钙俗名生石灰,某同学 针对氧化钙设计了如下实验方案:
针对氧化钙设计了如下实验方案:

(1)A中发生反应的化学方程式为___________。分离B中难溶物的操作I叫_________。
(2)如果要用实验证明C中不是水而是一种溶液,可以选择下列______(填序号)进行试验。
①稀盐酸 ②酚酞溶液 ③二氧化碳 ④氯化钠溶液
(3)操作II是加入某种物质使无色澄清液出现白色固体,如果加入的是饱和碳酸钠溶液,白色固体的化学式是___________;如果加入的是固体氢氧化钠(全部溶解),白色固体的化学式是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
某小组在学习“二氧化碳制取的研究”课题时,探究了二氧化碳气体的收集方法。
【查阅资料】
通常状况下,1 体积水约能溶解1 体积二氧化碳,所得溶液PH 约为5.6。
【提出问题】
二氧化碳能不能用排水法收集?
【实验设计与操作】
实验一、在通常状况下,测定二氧化碳溶液水所得溶液调查PH,判断二氧化碳在水中溶解度的体积。
(1)甲装置中反应的化学方程式是 。
(2)实验时,需先将甲装置中的空气排尽。其操作是:开启弹簧夹 、关闭弹簧夹-----,打
开活塞,滴加稀盐酸至空气排尽。检验空气已排尽的方法是 .
(3)关闭K1,打开K2,K3。待丙装置中收集半瓶气体时,关闭活塞K2 和K3,充分振荡丙装置。然后用pH 计测得如下数据:
| 物质 | 丁装置中溶液 | 丙装置中溶液 |
| pH | 6.50 | 5.60 |
分析可知,在丙和丁装置中所溶解二氧化碳的体积 (填“大于”“小于”“等于”) 丙和丁装
置中溶液的总体积。
(4)实验中,乙装置的作用是 。若没有乙装置,则测出的溶液pH 会 。
实验二:在通常状况下分别测定排空气法和排水法收集的气体中氧气的体积分数,从而得到二氧化碳的体积分数。
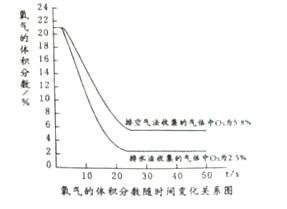
(5)用氧气测量仪测得收集的气体中氧气体积分数随时间的变化关系如图(起始时氧气的体积分数都以21%计),则最终两种方法收集的气体中二氧化碳体积分数较大的是 (填“排空气”或“排水”)法,两种方法收集的气体中二氧化碳体积分数的差值是 。
【结 论与反思】
论与反思】
(6)由实验 一、二分析,你认为二氧化碳 (填“能”或“不能”)用排水法收集,能减少二氧
一、二分析,你认为二氧化碳 (填“能”或“不能”)用排水法收集,能减少二氧
化碳在水中溶解度的措施是 。(写一条即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
现有锌和另一种金属组成的混合物,把6.5g该混合物加入到足量的稀硫酸中,恰好完全反应,产生氢气的质量为w.则下列说法中正确的是( )
A.该混合物可能是Zn、A1,w可能是0.2g
B.该混合物可能是Zn、Fe,w可能是0.2g
C.若混合物为Zn、Cu,w是0.1g,则该混合物中锌的质量分数为50%
D.若混合物为Zn、Mg,w是0.1g,则该混合物中锌的质量分数为50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com