
分析 (1)氮气的沸点比氧气的沸点低;
(2)分子、原子的种类都很多,无法比较直径大小;
(3)根据构成物质的微粒之间有间隙进行分析;
(4)根据组成比较甲醛、醋酸中碳元素的质量分数.
解答 解:(1)在同温同压下,液氮的沸点小于液氧的沸点;
(2)分子、原子的种类都很多,无法比较直径大小;
(3)分子之间有间隙,酒精和水混合物,酒精分子和水分子会进入到彼此的分子间隙之中,所以体积会减小;
(4)在葡萄糖、醋酸组成中碳、氢、氧个元素原子的个数比都是1:2:1,所以,甲醛、醋酸中碳元素的质量分数相等.
故答为:(1)A;(2)D; (3)B; (4)C.
点评 本题考查知识面全,需要同学们具有较为综合的化学知识和细心的能力才可做好.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:初中化学 来源: 题型:解答题
| 物质 | X | Y | Z | W |
| 反应前质量/g | 10 | 3 | 90 | 0 |
| 反应后质量/g | 3.2 | 3 | a | 3.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -5 | B. | +2 | C. | +3 | D. | +5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 缺铁会引起贫血 | B. | 缺碘会引起龋齿 | ||
| C. | 缺钙会引起骨质疏松 | D. | 缺锌会引起发育停滞得侏儒症 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 学习CO2性质后甲同学设计了《铁树开花》趣味实验,模拟医院看病情景给铁树“挂气治病”让其开红花.如图1所示:用盐水瓶收集了250mL CO2;如图2所示:在铁丝树上穿四个用紫色石蕊试液浸泡过的棉花球,放入250mL的烧杯中.其中棉球 1、2、3为潮湿的,4是干燥的.
学习CO2性质后甲同学设计了《铁树开花》趣味实验,模拟医院看病情景给铁树“挂气治病”让其开红花.如图1所示:用盐水瓶收集了250mL CO2;如图2所示:在铁丝树上穿四个用紫色石蕊试液浸泡过的棉花球,放入250mL的烧杯中.其中棉球 1、2、3为潮湿的,4是干燥的.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中,不正确的是( )| A. | 药品没说明用量,红磷应取最少量 | |
| B. | 点燃红磷前先用弹簧夹夹紧乳胶管 | |
| C. | 红磷熄灭后冷却到室温再打开弹簧夹 | |
| D. | 红磷燃烧产生大量白烟,放出大量的热 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 操作 | 装置 | 现象 |
| 1.取一小块铜丝网,卷成筒形,固定在铜丝上. |  | |
| 2.分别向①和②中注入15mL、30%的过氧化氢,并放入盛有热水的③中. |  | 约1min后可观察到①和②中都有少量气泡产生. |
| 3.把铜丝网插入①中. | 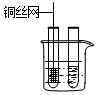 | ①中有大量气泡产生,5min后不再有气泡产生;此时②中仍然不断有少量气泡产生. |
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 时间(秒) | 22 | 13 | 12 | 10 | 9 | 8 | 5 | 3 | 3 | 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com