
 盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,有许多实验都用到盐酸.
盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,有许多实验都用到盐酸. 分析 (1)根据浓盐酸的挥发性分析;
(2)根据中和反应的原理书写方程式;根据指示剂的变色反应分析;根据盐酸的化学性质分析.
解答 解:(1)浓盐酸具有挥发性,打开瓶塞,瓶口会出现白雾,是因为挥发出的氯化氢气体结合空气中的水蒸气形成了盐酸的小液滴;故填:白雾;
(2)盐酸和氢氧化钠发生反应的方程式为:HCl+NaOH═NaCl+H2O;
氢氧化钠呈碱性,能使无色酚酞试液变红,加入盐酸的过程中要不断搅拌,使盐酸与氢氧化钠充分反应,防止局部酸液过量,酚酞在中性或酸性溶液中都显无色,当红色消失时说明盐酸与氢氧化钠发生了反应;
A、滴加石蕊,溶液变蓝,说明氢氧化钠过量,盐酸不足,故A错误;
B、若恰好完全反应,滴加氢氧化钠溶液,溶液颜色应变红,若不变色则说明盐酸过量,故B正确;
C、加蒸馏水不能起到任何作用,故C错误;
D、锌和盐酸反应生成氯化锌和氢气,有气泡产生,故D正确.
故填:HCl+NaOH=NaCl+H2O;溶液由红色变为无色;BD.
点评 本题考查了常见酸和碱的性质,明确中和反应指示剂的作用,掌握盐酸的性质是解题的关键.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:选择题
| A. | 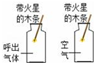 探究呼出气体和空气中氧气含量的不同 | |
| B. | 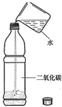 说明二氧化碳与水反应 | |
| C. | 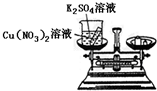 证明质量守恒定律 | |
| D. | 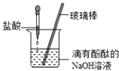 氢氧化钠能与盐酸反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 镁条在空气中久置表面会变黑,某小组同学设计并进行实验,探究镁条变黑的条件.
镁条在空气中久置表面会变黑,某小组同学设计并进行实验,探究镁条变黑的条件.| 编号 | 主要实验操作 | 实验现象 |
| 1 | 先充满用NaOH浓溶液洗涤过的空气再加入2mL浓硫酸 | 镁条始终无明显变化 |
| 2 | 加入2mLNaOH浓溶液 | 镁条始终无明显变化 |
| 3 | 先加入2mL浓硫酸再通入约4mLCO2 | 镁条始终无明显变化 |
| 4 | 先加入4mL饱和Na2SO3溶液再充满CO2 | 镁条始终无明显变化 |
| 5 | 先加入2mL蒸馏水再通入约4mLCO2 | 镁条第3天开始变黑至第20天全部变黑 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
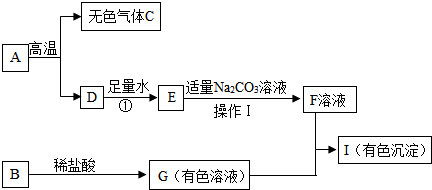
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失 | |
| B. | 在NaAlO2中铝元素的化合价为+3价 | |
| C. | 向稀盐酸中加入氢氧化铝,发生中和反应 | |
| D. | 氢氧化铝属于氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气 | B. | 二氧化硫 | C. | 二氧化碳 | D. | 一氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
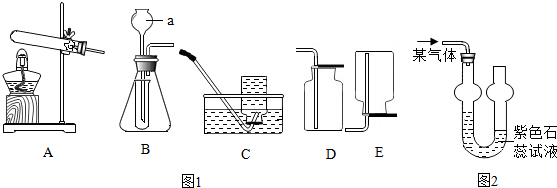
| O2 | HCl | NH3 | CO2 | |
| 通常情况下,1体积水 能吸收的气体的体积 | 0.031 | 500 | 700 | 1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
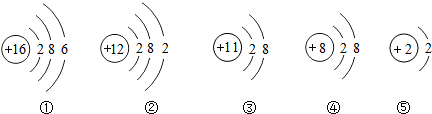
| A. | ①②属于第三周期元素,③④属于第二周期元素 | |
| B. | ③④、②⑤的化学性质相似 | |
| C. | ①元素最高正价为+6价,负价为-2价 | |
| D. | ①②表示的是原子,而③④⑤表示的是阴离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
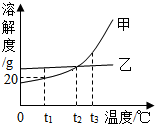 甲、乙两种不含结晶水的固体物质的溶解性曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解性曲线如图,下列说法中正确的是( )| A. | t2℃时,甲、乙两种饱和溶液中溶质的质量分数相等 | |
| B. | t1℃时,甲的饱和溶液中溶质与溶液的质量比为1:5 | |
| C. | 甲的溶解度比乙大 | |
| D. | 将等质量甲、乙的两种溶液分别由t3℃降温至t2℃,析出甲的质量一定比析出乙的质量大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com