
科目:初中化学 来源: 题型:解答题
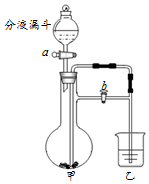 化学小组同学利用如图装置分别完成2个实验.
化学小组同学利用如图装置分别完成2个实验.| 序号 | 甲 | 乙 | 分液漏斗 |
| 1 | 大理石 | 澄清石灰水 | 稀盐酸 |
| 2 | 二氧化锰 | 80℃热水及一小块白磷 | 过氧化氢溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 材料对我们的生活影响越来越大
材料对我们的生活影响越来越大查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 100克水中含氯化钠15克 | |
| B. | 100克氯化钠溶液中含氯化钠15克 | |
| C. | 100克水中最多可溶解15克氯化钠 | |
| D. | 将溶液倒出一半后,质量分数变为7.5% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10m克 | B. | 20m克 | C. | 30m克 | D. | $\frac{1000a}{100-a}$克 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com