
 考前必练系列答案
考前必练系列答案科目:初中化学 来源: 题型:选择题
| A. | 倾倒液体时要将瓶盖倒放在桌面上,标签朝着手心 | |
| B. | 用托盘天平称取5.43g氯化钠 | |
| C. | 过滤时,将玻璃棒靠在三层滤纸的一边 | |
| D. | 用10mL量筒量取9.5mL液体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
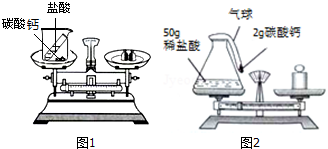
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭在氧气中燃烧生成二氧化碳 | |
| B. | 红磷在空气中燃烧产生大量白色烟雾 | |
| C. | 硫磺在空气中燃烧发出淡蓝色火焰 | |
| D. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是由氢、氧两种原子组成 | B. | 实验室可通过电解水制备H2 | ||
| C. | 明矾可以降低水的硬度 | D. | 水是一种良好的溶剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:
1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com