
【题目】如图是化学实验中常用的几种装置.

请回答下列问题:
(1)指出有编号的仪器名称:①___.
(2)写出实验室利用上述A装置制取氧气的化学反应方程式___.
(3)若用F装置干燥生成的氧气,F中盛放的液体试剂是___,气体应从___端导入(填“a”或“b”).
(4)用KClO3制氧气时需加MnO2作催化剂.若在KClO3中加少量的KMnO4,也能加快KClO3的分解.用文字说明其原因___.
(5)写出用石灰石和稀盐酸制取二氧化碳的化学方程式___,
使用G装置制取该气体的突出优点是___,收集二氧化碳气体的装置是___;检验二氧化碳集满的方法是___.
【答案】长颈漏斗 ![]() (或
(或![]() ) 浓硫酸 a KMnO4受热分解生成二氧化锰,生成的二氧化锰做了氯酸钾的催化剂 CaCO3+2HCl=CaCl2+H2O+CO2↑ 可以控制反应的发生和停止 D 将燃着的木条放在集气瓶口,如果木条熄灭,则证明已满
) 浓硫酸 a KMnO4受热分解生成二氧化锰,生成的二氧化锰做了氯酸钾的催化剂 CaCO3+2HCl=CaCl2+H2O+CO2↑ 可以控制反应的发生和停止 D 将燃着的木条放在集气瓶口,如果木条熄灭,则证明已满
【解析】
(1)根据实验室常用仪器可知:①长颈漏斗;
(2)实验室里用装置A为固体加热型装置,可用于氯酸钾或高锰酸钾制取氧气,反应的方程式为:![]() (或
(或![]() );
);
(3)浓硫酸具有吸水性,氧气可以用浓硫酸干燥,并且长进短出;气体应从a进;
(4)若在KClO3中加少量的KMnO4,也能加快KClO3的分解,是因为KMnO4受热分解生成二氧化锰,生成的二氧化锰做了氯酸钾的催化剂;
(5)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的方程式为::CaCO3+2HCl=CaCl2+H2O+CO2↑;用C装置制取二氧化碳,使用该装置制取气体的突出优点是:可以控制反应的发生和停止.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集。


科目:初中化学 来源: 题型:
【题目】可燃冰的分子结构类似于笼形,即若干个水分子将甲烷分子包裹在里面,其化学式为CH4·nH2O,n一般为6-8。仅我国南海可燃冰提供的能源就够中国用80年以上。
(1)甲烷是一种____(填“无机化合物”或“有机化合物”),属于____(填“可”或“不可”)再生能源。我国的可燃冰开采技术世界领先,若甲烷大量泄露到大气中,会加剧__(填一种大气危害现象)的产生;甲烷燃烧的化学方程式为__。
(2)海底的CH4在0℃、30个大气压的条件即可生成可燃冰,该反应的化学方程式是____;若n=8时,其中碳元素质量分数是____。
(3)可燃冰燃烧时能量转化形式主要是化学能转化为____能,而CH4—O2燃料电池则是将化学能转化为____能的装置;
(4)我国于2017年4月成功开采获取可燃冰,其意义在于____。
a.促进我国能源结构的快速转型
b.有助于中国在可燃冰可采和利用领域具备一定的话语权
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验创新小组对木炭还原氧化铜的实验进行了改进,

其操作步骤如下:①取一片铜片用砂纸除去其表面的氧化物,使其表面呈光亮的紫红色.
② 用酒精灯将上述铜片烧到红热后,立即伸到盛满氧气的集气瓶中,观察到的现象为:铜片表面变成______色;
③在一支干燥的大试管中装入一定量的经烘干处理过的木炭粉,再将经过② 处理过的铜片部分埋入木炭粉中;
④按如图所示的装置图连接好各种仪器
⑤加热大试管,其中发生反应的化学方程式为__________,当观察到澄清石灰水_________后,停止实验,此时应先___________,再______________.
⑥待试管冷却后,用镊子取出铜片,洗净后观察,回答问题
(1)填写上述各空.
(2)⑤中若先后颠倒,造成的后果可能是_______________
(3)⑥中观察到现象是:铜片表面埋入木炭粉中的部分________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将相同体积、相同溶质质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如右图所示。下列说法中正确的是
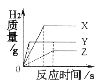
A.三种金属的活动性顺序为X>Z>Y
B.产生氢气的速率顺序为 X>Y>Z
C.反应完成时消耗稀盐酸的质量顺序为X>Y>Z
D.相对原子质量由大到小的顺序为 X>Y>Z
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一含有纯碱的食盐样品,为了测定其中碳酸钠的含量,某同学称取10g的样品放入烧杯中,向烧杯中加入100g足量的 稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为109.56g(假设产生的气体全部逸出。以下计算结果保留一位小数)
(1)样品中碳酸钠的含量是___
(2)NaCl中氯元素质量分数是____
(3)反应后溶液中溶质质量分数是___?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按要求写出相应的化学方程式
(1)有水参加的化合反应_____________________________。
(2)有水参加的分解反应 ____________________________。
(3)燃烧是一种常见的化学反应,根据你对燃烧反应的理解,试写出H2S气体充分燃烧的化学方程式_______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国著名化学家侯德榜发明的联合制碱法的主要原理是:向浓氨水中通入足量的CO2生成NH4HCO3(碳酸氢铵),然后加入食盐充分搅拌,两者发生复分解反应,由于碳酸氢钠的溶解度很小,便呈晶体析出,将析出的碳酸氢钠加热得碳酸钠,二氧化碳和水.
(1)请写出上述原理的三个化学方程式:
①_____;②_____;③_____.
(2)有人认为侯氏制碱法有以下优点,你认为正确的是_____.
A 生产过程中部分产物可作为原料使用 B 副产品是一种氮肥 C 反应不需要加热,可节约能源.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)从HCI、NaCl、NaOH、Na2CO3、Ca(OH)2几种溶液中取出其中的两种混合。
(1)若混合后溶液质量减小,可能的组合是________________。
(2)若混合的溶液质量不变,但发生了化学反应,有关的化学方程式为:________________、________________。
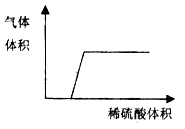
(3)将稀硫酸逐滴滴入剩下的几种组合中,若产生气体与加入稀硫酸有如图所示的关系,则这样的组合可能是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶过氧化氢溶液,标签如图。

试回答:
(1)实验室制取氧气时,通常要将30%的H2O2溶液稀释,其可能原因是_______。
(2)实验中需用6%的过氧化氢溶液100g,需30%的H2O2溶液体积为_____mL,加水为_________mL 。
(3)某同学取6.8g上述稀释后的溶液,用KMnO4溶液来测定其浓度,反应的化学方程式为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+SO2↑+8H2O,恰好完全反应时消耗溶质KMnO4质量为0.632g,计算稀释后溶液的实际浓度_________(写出计算过程)。
(4)若溶液稀释过程是正确的,则实际浓度偏低的可能原因是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com