
| 操作 | 现象 | 结论 |
| 取洗净后的白色固体,加入足量的 | 观察到 | 白色固体一定含有MgCO3 |
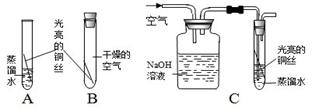
| 秤取一定量白色固体,充分加热至不再产生气体,将产生的气体先通入碱石灰,再通入浓硫酸,分别称量装置反应前后的质量 | 碱石灰增重,浓硫酸不变 | |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的 | | 猜想一 正确 |
| 步骤2:将步骤1试管中的混合物过滤,向滤液中滴加无色酚酞溶液 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验 | X放入稀硫酸中 | Zn放入稀硫酸中 | Cu放入稀硫酸中 |
| 实验现象 | 金属X表面产生气泡缓慢 | 金属锌表面产生气泡较快 | 金属铜表面无气泡 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量的滤液于试管中,在滤液中加入 。 | | 猜想②成立 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
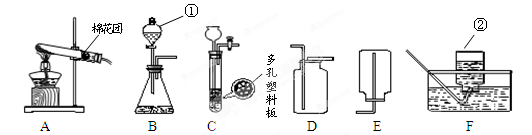
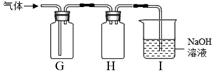
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
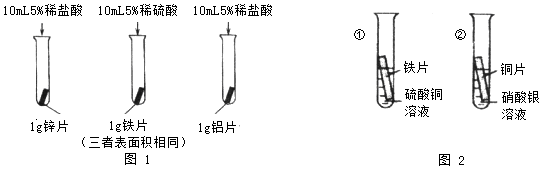
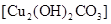 。他们依照钢铁生锈的探究方法设计如下实验(下图3所示)。请回答:
。他们依照钢铁生锈的探究方法设计如下实验(下图3所示)。请回答: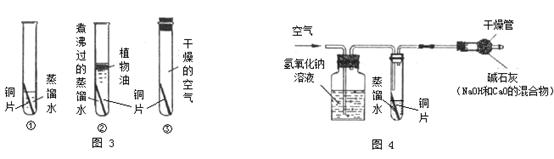
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
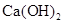 溶液、Na2CO3溶液中的一种。请你将它们区分出来,并完成下面的实验报告。
溶液、Na2CO3溶液中的一种。请你将它们区分出来,并完成下面的实验报告。| 实验步骤 | 实验现象 | 实验结论与解释 |
Ⅰ. 分别取四种待测液于4支试管中并编号,再分别向其中滴加无色的________溶液(如下图),振荡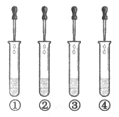 | ①②③中的溶液均由无色变为红色 ④中无现象 | ①②③中溶液显________(填“酸”或“碱”)性 ④中的原试剂瓶中的溶液是________ |
| Ⅱ. 向上述所得①②③的溶液中分别加入已区分出的④溶液 | 三支试管中的溶液均由红色变为无色,①中还伴有的现象是________;②③中无其他现象 | ①中原试剂瓶中的溶液是Na2CO3溶液 步骤Ⅱ后①中的溶质可能是________________(除指示剂外) |
| Ⅲ. 向步骤Ⅱ后所得②③的溶液中,分别滴加过量的①中原试剂瓶中的溶液 | ②中先有无色气泡,出现白色沉淀,溶液由无色变为红色 | ②中原试剂瓶中的溶液是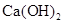 溶液 溶液 |
| ③中的现象可能是_________ ___________________ | ③中原试剂瓶中的溶液是NaOH溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象及结论 |
| | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
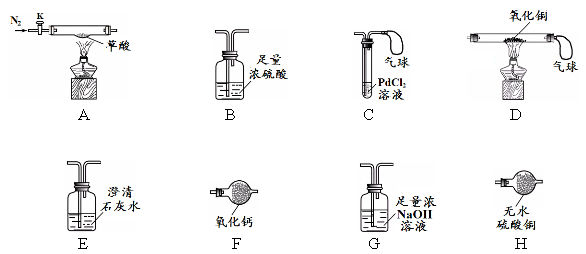
| 实验步骤 | 实验现象 | 实验结论及分析 |
| (1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 | H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 | 草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
| 实验步骤 | 实验数据 | 实验结论及分析 |
| (1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 | B装置增重1.8 g D装置中固体质量减少0.8 g G装置增重4.4 g | ①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com