
������(Na2SiO3)���ҹ����ȷ�չ�ľ�ϸ������Ʒ����ҵ�Ʊ��ķ�ӦΪ�� 2NaOH+ SiO2 == Na2SiO3 + H2O ������125tʯӢɰ(SiO2��������Ϊ96��)Ϊԭ�ϣ���������NaOH��Һ��Ӧ���Լ��㣺
(1)125tʯӢɰ��SiO2������Ϊ____________��
(2)�����ϵõ������Ƶ�����Ϊ____________��
120t 244t �������������ȸ���ʯӢɰ��������ʯӢɰ��SiO2���������������SiO2�������ٸ��ݷ�Ӧ�Ļ�ѧ����ʽ������SiO2���������㷴Ӧ�����ɹ����Ƶ������� �������� ��1��ʯӢɰ�е�SiO2��������125t��96%��120t ��2�������ɹ����Ƶ�����Ϊx 2NaOH + SiO2 = Na2SiO3 + H2O 80 122 120t x ...
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ2018���п���ѧ�Ծ� ���ͣ���ѡ��
ɫ����(C11H12N2O2)�ǰ������е�һ�֣��������ں���̫�ͻ�Ӱ��˯��������һ���ͨ��ʳ���ƶ�����֥�顢��з�����ɵȵ��Ը��ơ��й�ɫ�����������ȷ����
A. ���ķ����ں�����Ԫ�� B. �����е�����
C. ��������27��ԭ�� D. ���е�̼������������ij���Ԫ��
D ��������A�����ķ����ں�����ԭ�ӣ�����B��ɫ�����к��е�Ԫ�أ�����C��һ��ɫ������ӹ�����27��ԭ�ӣ�����D����������ij���Ԫ����̼���⡢�����������ס��ȡ��ơ��ء��ơ�þ����11�֣���ȷ����ѡD���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ������2018���п���ѧ���� ���ͣ���ѡ��
��ͼ�Ǽס��ҡ�������������ˮ�е��ܽ�����ߡ�����˵����ȷ����( )

A. t2��ʱ�ܽ���ɴ�С��˳������>��>��
B. ��t2�潵��t1���������������Ǽ���Һ
C. ��t2�潵��t1�����ҺŨ��һ���������仯
D. ���ұ����������ܽ�ȶ����¶����߶�����
C ��������A�������ܽ�����߿�֪����t2��ʱ���������ʵ��ܽ�ȴ�С��ϵ�Ǽף��ң�������A����B�����ڼ��ҵ��ܽ�����¶ȵĽ��Ͷ���С����˽���ʱ�����ʵı�����Һ�ж����о������������ڲ�֪����Һ��������״̬������������Ķ������Ƚϣ����ڱ����ܽ�����¶ȵĽ��Ͷ�������˽���ʱ������Һ�в����о�����������B����C�����ڱ����ܽ�����¶ȵĽ��Ͷ�������˽���ʱ������Һ�в����о�������������...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ����������2018����꼶�п�ģ�⻯ѧ�Ծ� ���ͣ������
��Ƕ���ʶ���ʣ��ܰ������Ǹ�ȫ���˽��������硣�������Ͷ�����̼Ϊ�����ش��������⣺
��1����ʶ���ʵ���ɺͽṹ
�ٴӺ���Ͽ��������Ͷ�����̼������__�����Ԫ�ء� �������ӡ�����
�ڴ����Ͽ��������Ͷ�����̼����___���ɡ����Ԫ�ء� ���ӡ���
��2����ʶ���ʵ�����

�ٽ�պ�оƾ�����о��ȼ�����ձ��У����ձ��л����㵹������̼���۲쵽�ձ��е���о���¶���Ϩ����ͼ��ʾ��˵��������̼���е�������_________��
����ʹ��о�°�λָ�ȼ�գ�����������_______��
��3����֤����ʶ����
��������ۡ��ӡ�������̼��������ЧӦ������ʵ��������������ʹȫ�������ů���º�ƽ�������ȣ���������Ϊ��ҵ������ֲ��Ĺ�������ṩ�ḻ��ԭ�ϡ�ֲ�������õĻ�ѧ����ʽΪ��6CO2+6H2O 6O2+X����X�Ļ�ѧʽ��____���̶������ö�����̼�ijɹ������ǣ��ڸ��¡���ѹ�£��Զ�����̼�Ͱ�����NH3��Ϊԭ�Ϻϳ�����[CO(NH2)2]��ͬʱ��ˮ���ɣ���д���÷�Ӧ�Ļ�ѧ����ʽ��___��
6O2+X����X�Ļ�ѧʽ��____���̶������ö�����̼�ijɹ������ǣ��ڸ��¡���ѹ�£��Զ�����̼�Ͱ�����NH3��Ϊԭ�Ϻϳ�����[CO(NH2)2]��ͬʱ��ˮ���ɣ���д���÷�Ӧ�Ļ�ѧ����ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ����������2018����꼶�п�ģ�⻯ѧ�Ծ� ���ͣ���ѡ��
��ȷ��ʵ�������ʵ������������ȫ�dz���Ҫ������ʵ�������ȷ����( )
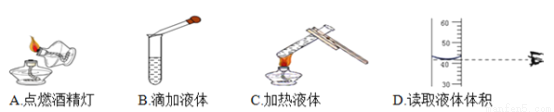
A. A B. B C. C D. D
D ��������A����ֹ�þƾ�����ȼ��һֻ�ƾ��ƣ�����B���ι����Թ��Ϸ����մ�ֱ������C���Թ����Һ�岻�ܳ����Թ��ݻ��ģ�����D�������밼Һ�����ʹ�����ˮƽ����ȷ����ѡD���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㶫ʡ������������ͬʤѧУ2018����꼶�п�ģ�⻯ѧ�Ծ� ���ͣ���ѡ��
����ѡ�����ͼʾ������ϵ����
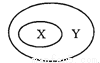
A | B | C | D | |
X | ���� | ���ֽⷴӦ | ������ | ��ʯȼ�� |
Y | ���� | ���Ϸ�Ӧ | ������ | ʯ�� |
A. A B. B C. C D. D
A ��������A�����ʰ�������������ǽ������ʣ�Ӧ��X������Y����ȷ��B�����ֽⷴӦ�뻯�Ϸ�Ӧ�Dz��й�ϵ������C���������Ϊ���ʺͻ����ӦΪY������X������D����ʯȼ����Ҫ�����֣�ú��ʯ�͡���Ȼ����ӦΪY������X������ѡA���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��������ҵˮƽ�߸�����������ģ�⻯ѧ�Ծ� ���ͣ���ѡ��
�ֵ�Ͳ��ʹ�õ�п���̸ɵ�أ��ڹ���ʱ�����Ļ�ѧ����ʽΪ��Zn + 2NH4Cl + 2MnO2 === ZnCl2 + 2NH3 �� +X + H2O����X �Ļ�ѧʽΪ( )
A. MnO B. HMnO4 C. Mn3O4 D. Mn2O3
D ����������ѧ��Ӧǰ�����ԭ�Ӹ�����ȣ���Ӧǰ��Zn ��2N��8H��2Cl ��2Mn��4O����Ӧ��X������Zn��2Cl�� 2N��8H ��O������һ��X�����к���2Mn��3O��X�Ļ�ѧʽΪMn2O3����ѡD���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��������ʡ��������2018���п���ѧ�Ծ� ���ͣ���ѡ��
ʵ������һ�������ʵ�̼��������Ʒ100g(���ʲ�����Ԫ�أ����Ȳ��仯)��������Ԫ����������Ϊ23%��180��ʱ������Ʒ����һ��ʱ���Ƶù�������Ϊ87.6g����ֽ��̼������ռԭ̼�����Ƶ���������Ϊ(2NaHCO3 Na2CO3 + H2O + CO2��)
Na2CO3 + H2O + CO2��)
A. 33.6% B. 40% C. 47.3% D. 60%
B ������������Ʒ��̼�����Ƶ�����������x����100g��x��=100g��23%�����x=84% ��Ʒ��̼�����Ƶ�����Ϊ��100g��84%=84g ��ֽ��̼�����Ƶ�������y 2NaHCO3Na2CO3 + H2O + CO2�� ��Ӧǰ�����IJ��� 2��84 106 2��84-106=62 y 100g-87.6g=12.4g =�����y=33.6g ...�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com