
分析 a.显碱性的溶液能使酚酞试液变红色;
(二)氢气燃烧能够产生淡蓝色火焰,不能与氢氧化钙反应;
【作出猜测】根据质量守恒定律可以判断物质的组成情况;
【设计并进行实验】
碳酸镁能和稀盐酸反应生成氯化镁、水和二氧化碳;
通过计算可以判断物质的质量比.
解答 解:a.溶液红色加深,则反应后溶液的碱性增强.
故填:增强.
b.(1)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为氢气,氢气的化学式是H2.
故填:H2.
【作出猜测】②白色固体可能是MgCO3,白色固体可能是Mg(OH)2,白色固体可能是MgCO3和Mg(OH)2.
故填:Mg(OH)2.
【设计并进行实验】
(1)取洗净后的白色固体,加入足量的稀盐酸溶液,观察到有气泡产生,则白色固体一定含有MgCO3.
故填:稀盐酸;有气泡产生.
(2)碳酸镁受热分解生成氧化镁和二氧化碳,氢氧化镁受热分解生成氧化镁和水,分解产生的气体全部先通过浓硫酸,浓硫酸增重,说明白色固体中含有氢氧化镁,再通过碱石灰,发现碱石灰明显增重了,说明白色固体中含有MgCO3.
答案:
a.增强
b.H2
【作出猜测】②Mg(OH)2.
【设计并进行实验】
(1)稀盐酸 有气泡产生
(2)Mg(OH)2,MgCO3
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:初中化学 来源: 题型:解答题
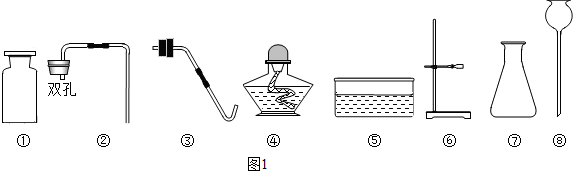

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
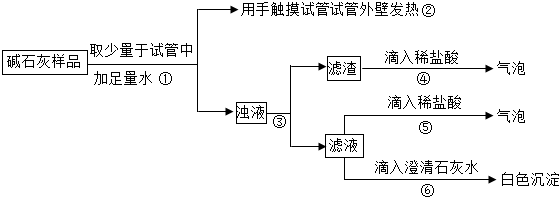
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生成的气体一定是过氧化氢分解产生的氢气 | |
| B. | 伤口处的生物酶可能对过氧化氢的分解起到催化作用 | |
| C. | 只有二氧化锰能使过氧化氢的分解速率加快 | |
| D. | 过氧化氢和水的分子构成不同,所以它们的性质完全不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
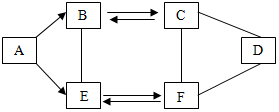 A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示(图中“-”表示反应关系,“→”表示转化关系,部分反应物、生成物及反应条件已略去).已知A、B、C、D、F是不同类别的物质,A、B分别为气体,A是单质,E是相对分子质量最小的氧化物.请回答:
A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示(图中“-”表示反应关系,“→”表示转化关系,部分反应物、生成物及反应条件已略去).已知A、B、C、D、F是不同类别的物质,A、B分别为气体,A是单质,E是相对分子质量最小的氧化物.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com