
【题目】请完成以下填空:
(1)在化学反应里,参加反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这就是_____________________________。
(2)由两种元素组成且其中一种是__________元素的化合物称为氧化物。
(3)下列玻璃仪器能直接加热的是_______(填仪器名称),仪器⑥的名称是___________。

(4)端午节的粽子煮熟后,往柴火上浇水使火熄灭,所用的主要灭火原理是______________;吃完粽子后手上粘有油污,用洗洁精洗去油污时,洗洁精起到________________作用。
(5)下表为元素周期表前四周期的部分信息。A元素在周期表①位置,请画出它的原子结构示意图________,它与表中②位置的元素组成化合物的化学式为____________。
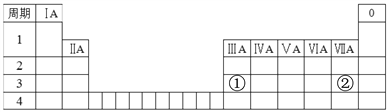
(6)在粗盐提纯过程中,将氯化钠溶液蒸发至有较多固体析出后,应________________,并用玻璃棒不断搅拌,利用余热将余下水分蒸干。
(7)由相同元素组成的不同物质会体现出不同的性质。如:金刚石、石墨、C60的物理性质不同,其原因是______________________________________;一氧化碳和二氧化碳的化学性质不同,其原因是 _________________________________。
(8)用“![]() ”表示氧原子,“
”表示氧原子,“![]() ”表示氢原子;由它们构成的甲物质发生反应的微观示意图如图所示:
”表示氢原子;由它们构成的甲物质发生反应的微观示意图如图所示:
![]()
甲 乙 丙
则参加反应的甲与生成的乙和丙之间的分子个数比为_______。
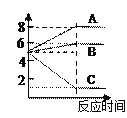
(9)把A、B、C三种物质各5 g放在试管内加热,充分反应后,这三种物质的质量前后变化如图所示,则它们发生的反应类型属于__________________(填“基本反应类型”)。
(10)已知镁原子的相对原子质量是24,一个C-12原子的质量约为1.993×10-26kg,那么一个镁原子的实际质量约为__________________kg。
(11)如图是A、B、C三种固体物质的溶解度曲线,据图回答下列问题:
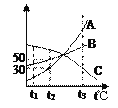
①在t2℃时,加水分别将30 g物质A和50 g物质B完全溶解,配制成饱和溶液,则物质A所需水的质量_____________物质B所需水的质量(填“大于、等于、小于”);
②分别将这三种物质在t3℃时的饱和溶液降温到t1℃时,这三种溶液中溶质的质量分数由大到小的排列是______________。
【答案】 质量守恒定律 氧 试管 量筒 降低温度到柴火的着火点以下 乳化 ![]() AlCl3 停止加热 碳原子的排列方式不同 分子构成不同 2︰2︰1 分解反应 3.986×10﹣26 等于 B C A或 B→C→A
AlCl3 停止加热 碳原子的排列方式不同 分子构成不同 2︰2︰1 分解反应 3.986×10﹣26 等于 B C A或 B→C→A
【解析】(1)质量守恒定律是指:在化学反应里,参加反应的各物质的质量总和,等于反应后生成的各物质的质量总和;(2)氧化物是指:由两种元素组成且其中一种是氧元素的化合物称为氧化物;(3)根据常见仪器的辨认,可以直接加热的仪器是试管,图中仪器⑥的名称是:量筒;(4)往柴火上浇水使火熄灭,是将温度降低至着火点以下,洗洁精洗去油污是利用的是乳化原理;(5)根据元素周期表信息及排列规律可知,图中位置①的元素是13号元素![]() ,其原子结构示意图为:
,其原子结构示意图为:![]() ,图中位置②的元素是17号元素
,图中位置②的元素是17号元素![]() ; 13号元素
; 13号元素![]() ,最外层电子数为3,容易失去,带3个单位的正电荷,化合价为正三价,17号元素
,最外层电子数为3,容易失去,带3个单位的正电荷,化合价为正三价,17号元素![]() ,最外层电子数为7,容易得到1个电子,带一个单位的负电荷,化合价为-1价,根据化学式书写原则可知,其化学式为:
,最外层电子数为7,容易得到1个电子,带一个单位的负电荷,化合价为-1价,根据化学式书写原则可知,其化学式为: ![]() ;(6)在粗盐提纯过程中,将氯化钠溶液蒸发至有较多固体析出后,应停止加热,并用玻璃棒不断搅拌,利用余热将余下水分蒸干;(7)金刚石、石墨、C60的物理性质不同是因为碳原子的排列方式不同,金刚石呈正八面体结构,石墨呈层状结构,
;(6)在粗盐提纯过程中,将氯化钠溶液蒸发至有较多固体析出后,应停止加热,并用玻璃棒不断搅拌,利用余热将余下水分蒸干;(7)金刚石、石墨、C60的物理性质不同是因为碳原子的排列方式不同,金刚石呈正八面体结构,石墨呈层状结构, ![]() 呈足球状;一氧化碳和二氧化碳的化学性质不同,其原因是分子的构成不同;(8)由上图可知,过氧化氢分解生成水和氧气,其化学反应方程式为:
呈足球状;一氧化碳和二氧化碳的化学性质不同,其原因是分子的构成不同;(8)由上图可知,过氧化氢分解生成水和氧气,其化学反应方程式为: ![]()
![]()
![]() ,所以参加反应的甲与生成的乙和丙之间的分子个数比为2:2:1;(9)从示意图提供的信息可知,A、B反应后质量增加,为生成物,C反应后质量减少,为反应物;反应物为一种,生成物为两种,故该反应为分解反应。(10)根据
,所以参加反应的甲与生成的乙和丙之间的分子个数比为2:2:1;(9)从示意图提供的信息可知,A、B反应后质量增加,为生成物,C反应后质量减少,为反应物;反应物为一种,生成物为两种,故该反应为分解反应。(10)根据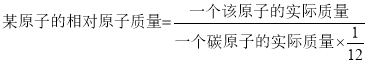 ,设一个镁原子的质量为
,设一个镁原子的质量为![]() ,则
,则![]() ,
, ![]() ;(11)①根据图示可知,在t2℃时, 30 g物质A溶于100g水中形成饱和溶液,50 g物质B溶于100g水中也能形成饱和溶液,故在t2℃时,加水分别将30 g物质A和50 g物质B完全溶解形成饱和溶液,需加入水的质量相等;②分别将这三种物质在t3℃时的饱和溶液降温到t1℃时,A、B的溶解度降低,有晶体析出,且A析出晶体的量大于B,溶质质量是B>A,而C物质的溶解度增大,没有晶体析出,溶质质量不变,质量分数不变,从图示可以看出:三者的质量分数大小为:B→C→A。
;(11)①根据图示可知,在t2℃时, 30 g物质A溶于100g水中形成饱和溶液,50 g物质B溶于100g水中也能形成饱和溶液,故在t2℃时,加水分别将30 g物质A和50 g物质B完全溶解形成饱和溶液,需加入水的质量相等;②分别将这三种物质在t3℃时的饱和溶液降温到t1℃时,A、B的溶解度降低,有晶体析出,且A析出晶体的量大于B,溶质质量是B>A,而C物质的溶解度增大,没有晶体析出,溶质质量不变,质量分数不变,从图示可以看出:三者的质量分数大小为:B→C→A。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A.燃烧是人类最早利用的化学反应之一
B.可燃物温度达到着火点即可燃烧
C.图书档案起火宜用水基型灭火器扑灭
D.不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)要配制50 g溶质质量分数为11%的氯化钠溶液,需要水的体积为_________mL(水的密度是1 g·mL-1);
(2)下列配制氯化钠溶液的过程图组顺序有误且不全,请将⑦框内所缺的实验步骤图用文字补全在横线上_____________________;
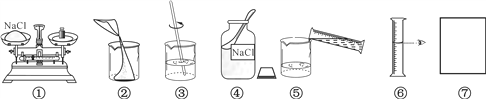
(3)小明同学按(1)和(2)的正确实验步骤配制好溶液后,发现所配制的氯化钠溶液溶质的质量分数小于11%,造成溶质质量分数偏小的原因可能是_______(填序号)。
A.称量时药品和砝码放反了 B.量取水时仰视量筒读数
C.所取用的氯化钠含有杂质 D.称量好的溶质倒入烧杯时有部分洒出
(4)金属与酸反应的剧烈程度反映了金属活动性的强弱。把形状、大小相同的纯金属
A、B、C、D同时放入装有足量稀盐酸的烧杯中,以下卡通图形象地表现了此实验现象,由下图可知,活动性最强的金属是______(填字母代号)。
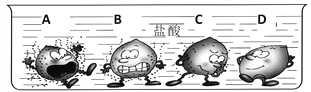
(5)请你写出锌与稀盐酸反应的化学方程式:_______________________。
(6)如图所示,将一支充满二氧化碳气体的试管倒插入氢氧化钠溶液中,一段时间后试管内液面上升了,请用化学方程式表示所发生的化学反应:________________________________。
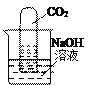
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体代谢产生的过氧化氢,对人体有毒害作用。人体肝脏中的过氧化氢酶能催化过氧化氢分解产生氧气和水。某同学查阅资料发现,FeCl3也能催化过氧化氢分解。为比较过氧化氢酶(其活性与温度有关,一定范围内促进,温度过高就使酶的活性降低)和FeCl3催化效率的高低,该同学在28℃环境下进行了如下探究:
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设:______________。
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),适宜浓度的过氧化氢溶液等。
(4)实验步骤:
①取2支洁净的试管,编号为1、2,并各注入3mL适宜浓度的过氧化氢溶液;
②向1号试管内滴入2滴适宜浓度的FeCl3溶液,向2号试管内_____________;
③观察并记录两支试管产生气泡的情况。
(5)预测实验结果:请写出一种可能的实验结果:____________________。
(6)在以上探究的基础上,该同学又完成了“探究温度对猪肝研磨液和FeCl3催化效率的影响”实验。实验结果如图所示。图中代表猪肝研磨液催化效率的曲线是____,判断的理由是__________。
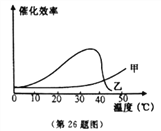
(7)写出1号试管内发生反应的文字表达式为__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
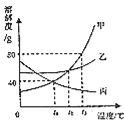
【题目】如图是常见固体物质的溶解度曲线,根据图示回答:
(1)在______℃时,甲和乙两种物质的溶解度相等.
(2)t1℃时,将140g甲的饱和溶液升温至t3℃时,需要加入______g甲物质,才可能形成饱和溶液.
(3)t3℃时,甲、乙、丙三种物质饱和溶液中溶质的质量分数由大到小的顺序是______.
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温至t1℃,没有晶体析出的是______(填“甲”、“乙”、“丙”).
(5)当甲中含有少量乙时,可以通过______的方法提纯甲.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】改进教材实验有利于充分发挥实验教学功能,培养创新能力。
【魔棒生烟】图1为教材实验:蘸有浓盐酸和浓氨水的玻璃棒靠近时产生白烟。图2为改进设计。

(1)图1实验说明分子____________。
(2)图2改进设计的优点是___________。
【测定空气中O2的体积分数】图3为教材实验,图4为改进设计。
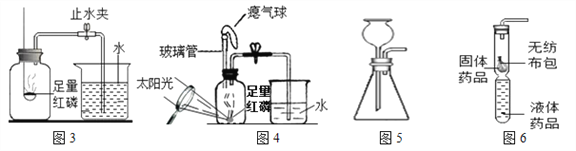
(3)实验中可以观察到红磷燃烧发出黄色火焰,放出大量的热并产生__________。
(4)图4改进设计中瘪气球的作用是____________。
(5)图4改进设计实验过程中瘪气球的变化情况是____________。
【实验室制取CO2】图5为教材中制取CO2的发生装置,图6是用软塑料管自制的气体发生装置。
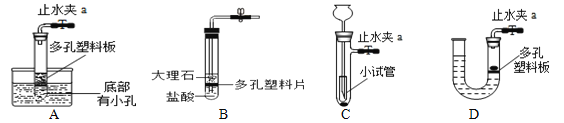
(6)图6改进设计的优点是_______________。
(7)下图装置中具有图6装置相同优点的是______________(选填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com