
【题目】某兴趣小组利用下列装置进行气体的制取实验,请回答下列问题.
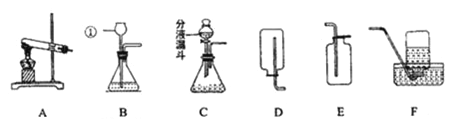
(1)写出标号①仪器的名称_________________.
(2)用高锰酸钾制取和收集较纯净的氧气,选择的装置组合是____________(填字母)还需补充的实验用品是______________,写出反应的化学方程式_________________,试验后发现制得的氧气不纯,可能的原因是_________________.(答一点即可)
(3)实验室制取二氧化碳的化学方程式_________________,与B相比,C作为制取二氧化碳的发生装置,优点是_________________,验证二氧化碳收集满的方法是_________________。
【答案】(1)长颈漏斗;(2)AF,棉花,2KMnO4![]() K2MnO4+MnO2+O2↑,收集的时刻过早;
K2MnO4+MnO2+O2↑,收集的时刻过早;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑,控制反应的速率,将燃着的木条放在集气瓶口,木条熄灭,证明气体集满。
【解析】
试题分析:(1)通过分析题中所指仪器的作用可知,①是长颈漏斗;(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,排水法收集的氧气纯净,所以选择的装置组合是AF,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑,实验后发现制得的氧气不纯,可能的原因是收集的时刻过早;(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl = CaCl2+H2O+CO2↑,分液漏斗可以控制液体的滴加速度,所以与B相比,C作为制取二氧化碳的发生装置,优点是控制反应的速率,二氧化碳不具有助燃性,所以验证二氧化碳收集满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明气体集满。
K2MnO4+MnO2+O2↑,实验后发现制得的氧气不纯,可能的原因是收集的时刻过早;(3)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl = CaCl2+H2O+CO2↑,分液漏斗可以控制液体的滴加速度,所以与B相比,C作为制取二氧化碳的发生装置,优点是控制反应的速率,二氧化碳不具有助燃性,所以验证二氧化碳收集满的方法是:将燃着的木条放在集气瓶口,木条熄灭,证明气体集满。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:
【题目】如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
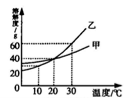
A.通过升温可以将甲的不饱和溶液变为饱和溶液
B.20℃时分别将甲、乙的溶液蒸发相等质量的水,析出甲、乙的质量相等
C.10℃时,10g水中分别溶解甲、乙达到饱和,溶解较多的物质是乙
D.把100g溶质质量分数为10%的乙溶液从30℃降温到10℃其质量分数仍为10%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学活动小组在一次实验中进行了如图所示实 验:先向A中注入一定量氯化铁溶液,再注入一定量硫酸钠溶液,此过程中观察到的现象是(1) 。小组同学对无色溶液B产生了浓厚的兴趣,进行了进一步的探究活动。

【提出问题】B中含的离子有什么?
【实验探究】

【评价交流】甲同学结论(2) (填“正确”或“错误”);乙同学的探究过程不正确,理由是(3) 。
【实验结论】结合上述实验最终确定B中含有(4) (填离子符号),不含(5) (填离子符号)。
【归纳总结】由甲、乙、丙同学实验对比得出,确定溶液中可能存在的不同离子是否存在的方法是:可根据待测离子与所加试剂反应(6)
确定出存在的离子,同时推测出与(7)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图象中有关量的变动趋势与对应的叙述关系正确的是( )
|
|
A.将等质量的锌粉和铁粉,分别放入两份溶质质量分数相同且足量的稀盐酸中 | B.一定质量的红磷在密闭容器中燃烧 |
|
|
C.向久置在空气中已经部分变质的氢氧化钠溶液中逐渐滴加稀盐酸至过量 | D.加热一定质量的氯酸钾和二氧化锰混合物至完全分解 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是目前世界年产量最多的金属
(1)如图是一氧化碳还原氧化铁实验装置图,回答下列问题:
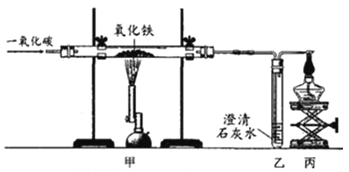
①写出甲处玻璃管中的化学反应方程式__________;
②下列关于该实验的说法正确的是__________(填字母)
A.装置甲处玻璃管内黑色粉末变红
B.实验结束后,应先熄灭甲处的酒精喷灯
C.一氧化碳发生了还原反应
(2)每年因腐蚀而浪费掉的金属材料数量惊人,铁栅栏常采取的防锈措施是__________,除防止金属腐蚀外,保护金属资源的有效途径还有__________(答一点即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在反应2A+B=3C+D中,A和B的相对分子质量之比为5:1,已知20gA与一定量B恰好完全反应,生成5gD,则在此反应中B和C的质量比为( )
A.4:19 B.3:5 C.1:3 D.2:17
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①人体缺乏后会引起贫血的元素____________;
②两个氢原子____________;
③三个二氧化硫分子 ____________;
④四个碳酸根离子____________。
(2)在符号“![]() O”中H正上方的“+1”表示____________,H右下角的“2”表示____________。
O”中H正上方的“+1”表示____________,H右下角的“2”表示____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示,FeCl3与NaOH反应的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl.请回答下列问题:
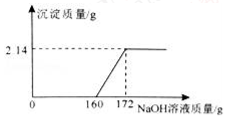
(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是 _________g.
(2)该工业盐酸中HCl的质量分数是多少?(写出计算过程)
(3)取l00g该工业盐酸稀释成HCl质量分数为10%的稀盐酸,需加多少克水?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com