
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:
| 实验步骤 | 简答 |
| (1)称取12.25克KClO3,加热至O2不再产生为止,用去20分钟,得到4.8克O2. | 写出方程式 |
| (2)取A克氧化铁加热,没有得到O2. | 氧化铁的化学式为 |
| 实验步骤 | 简答 |
| (3)将12.25克KClO3和A克氧化铁 混合物,加热至O2不再产生为止,用去8分钟,得到4.8克O2. | 反应中氧化铁的作用是 |
| (4)将步骤(3)试管内残余的固体进行分离,主要操作步骤有 |
可知反应前后氧化铁的 |
| (5)再将步骤(4)得到的氧化铁放入盛有足量稀盐酸的烧杯里,发现氧化铁消失,逐渐形成棕黄色溶液. | 实验说明分离后得到的氧化铁的 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| △ |
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | / | 67 | 1800 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | 67 | 89.5 |
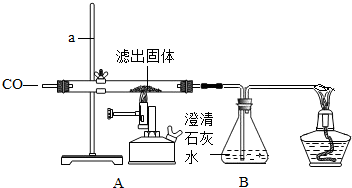
| 装置 | 实验现象 | 实验分析 |
| A | 红色固体全部变黑 | 生成了铁 |
| B | 石灰水变浑浊 | 产生二氧化碳 |
| 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 | |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与CO反应 | 不反应 | 反应 | 反应 | 反应 |
| 与稀盐酸反应 | 反应 | 生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 |
| 与硫酸铜溶液反应 | 反应 | 不反应 | 不反应 | 不反应 |
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | 剩余固体中没有氧化亚铁. | |
| 2 | 剩余固体中只有铁粉. |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 影响速率的 因 素 | 例 证 | 影响速率的 因 素 | 例 证 | 影响速率的 因 素 | 例 证 |
| 物质本身的 性 质 | 温 度 | 浓 度 | |||
| 催 化 剂 | 接触面积 | / | / |
查看答案和解析>>
科目:初中化学 来源:浦东新区一模 题型:问答题
| 实验步骤 | 简答 |
| (1)称取12.25克KClO3,加热至O2不再产生为止,用去20分钟,得到4.8克O2. | 写出方程式______ |
| (2)取A克氧化铁加热,没有得到O2. | 氧化铁的化学式为______ |
| 实验步骤 | 简答 |
| (3)将12.25克KClO3和A克氧化铁 混合物,加热至O2不再产生为止,用去8分钟,得到4.8克O2. | 反应中氧化铁的作用是______,生成氧气的质量为______. |
| (4)将步骤(3)试管内残余的固体进行分离,主要操作步骤有______、______和______.得到氧化铁的质量为______克. | 可知反应前后氧化铁的______保持不变. |
| (5)再将步骤(4)得到的氧化铁放入盛有足量稀盐酸的烧杯里,发现氧化铁消失,逐渐形成棕黄色溶液. | 实验说明分离后得到的氧化铁的______也保持不变. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
|
|
②氯酸钾和氯化钾均能溶于水。
【实验一】氧化铁能否在氯酸钾制取氧气实验中加快反应速率。
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 |
| 67 | 1800 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | g 氧化铁 | 67 | 89.5 |
⑴实验3中氧化铁的质量为 。
⑵以上实验采用了 的实验方法。
⑶实验一得到的结论是 。
【实验二】为证明氧 化铁是该反应的催化剂,同学们又完成了以下的实验:
化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤得到红色固体,洗涤干燥并用电子天平称量,质量为0.2g。
Ⅱ.将一定量的CO通入滤出的固体,按下图进行实验:
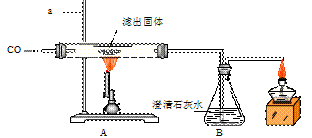
甲同学的实验 报告如下:
报告如下:
| 装置 | 实验现象 | 实验分析 |
| A | 红色固体全部变黑 | 生成了铁 |
| B | 石灰水变浑浊 | 产生二氧化碳 |
⑷写出A中玻璃管内发生反应的化学方程式 。
【实验结论】氧化铁能在氯酸钾制取氧气反应中起催化剂。
【实验反思】乙同学查阅资料发现一氧化碳还原氧化铁后剩余固体可能由氧化亚铁、四氧化三铁、铁粉和未反应的氧化铁中的一种或几种组成。
为了研究剩余固体的成分,丙同学查阅了以下资料:
| 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 | |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与CO反应 | 不反应 | 反应 | 反应 |
|
| 与稀盐酸反应 | 反应 | 生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 |
| 与硫酸铜溶液 | 反应 | 不反应 | 不反应 | 不反应 |
⑸丙同学认为剩余固体中一定没有氧化铁,原因是____________。
⑹测定剩余固体的组成。
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | _____________ | 剩余固体中没有氧化亚铁。 |
| 2 | __________________ | ______________ | 剩余固体中只有铁粉。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com