
分析 (1)该物质与参加反应的氧气的质量之和等于生成的二氧化碳和水的质量之和;
(2)根据反应前后元素种类不变;
(3)根据燃烧的化学方程式为R+02$\stackrel{点燃}{→}$C02+H20,利用质量守恒定律来推断R的化学式.
(4)化学反应前后,元素的种类不变,原子的种类、总个数不变;
化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.
解答 解:(1)根据质量守恒定律,参加反应的氧气的质量为:8.8g+5.4g-4.6g=9.6g.故填:9.6g;质量守恒定律.
(2)由题意“R在氧气中燃烧的化学方程式为R+O2$\stackrel{点燃}{→}$CO2+H2O”,可知:R中一定有C、H元素.
故填:R中一定有C、H元素;化学反应前后元素种类不变.
(3)解:在反应R+302$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H20,
根据质量守恒定律可知,
反应前后的元素种类、原子个数和种类不变,
反应后共2个C原子、6个H原子、7个O原子,
反应前现有6个O原子,
则X中共有2个C原子、6个H原子、1个O原子,
即该物质的化学式是C2H6O.故填:C2H6O;反应前后的元素种类、原子个数和种类不变;
(4)8.8g二氧化碳中氧元素的质量为:8.8g×$\frac{32}{44}$×100%=6.4g; 5.4g水中氧元素的质量为:5.4g×$\frac{16}{18}$×100%=4.8g;
参加反应的氧气质量为:8.8g+5.4g-4.6g=9.6g,
则该可燃物中氧元素的质量为:6.4g+4.8g-9.6g=1.6g,
二氧化碳中的碳元素和水中的氢元素来自于该可燃物,因此该可燃物中含有碳元素、氢元素和氧元素.
答案:碳、氢和氧;质量守恒定律.
点评 本题主要考查质量守恒定律和计算等方面的知识,化学方程式可以表示反应中各物质的质量比及构成各物质的粒子个数比,利用反应中的各种原子的个数关系是本题解答的一个重点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
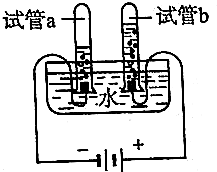
| A. | a试管中收集到的是一种可燃性气体 | |
| B. | b试管中收集到的气体能使带火星的木条复燃 | |
| C. | 该变化是分解反应 | |
| D. | a、b两试管内收集到的气体的质量之比约为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间(分钟) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 55 | 65 | 75 | 85 |
| 阳极生成气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com