
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:初中化学 来源: 题型:
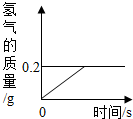 (2013?安庆二模)氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与水反应,得到100g氢氧化锂(LiOH)溶液,同时产生了氢气(LiH+H2O=LiOH+H2↑).产生氢气的质量与反应时间的关系如图所示,则所得氢氧化锂溶液的质量分数为多少?
(2013?安庆二模)氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与水反应,得到100g氢氧化锂(LiOH)溶液,同时产生了氢气(LiH+H2O=LiOH+H2↑).产生氢气的质量与反应时间的关系如图所示,则所得氢氧化锂溶液的质量分数为多少?查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
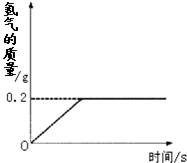 氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与99.4克水反应,产生气体的质量与反应时间的关系如图所示,请回答下列问题:
氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源.某化学兴趣小组取一定质量的氢化锂与99.4克水反应,产生气体的质量与反应时间的关系如图所示,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源,反应的化学方程式为:LiH + H2O LiOH + H2↑。计算80 g氢化锂与足量的水反应生成氢气的质量。
LiOH + H2↑。计算80 g氢化锂与足量的水反应生成氢气的质量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com