
科目:初中化学 来源: 题型:

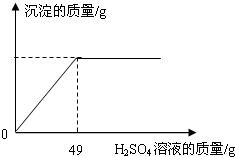
查看答案和解析>>
科目:初中化学 来源: 题型:
| 密 度/g?cm-3 | 1.01 | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
| 溶质的质量分数/% | 1 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 98 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 硫酸 体积:500mL 化学式:H2SO4 密度:1.4g/cm3 质量分数:50%(2)将20g合金粉末加入到98g新配好的稀硫酸中,恰好完全反应.过滤,将滤液蒸干后得到固体纯净物32.2g.通过计算回答: ①此合金为 ②写出发生反应的化学方程式: ③根据已知条件写出求解生成气体质量(x)的比例式: ④若向反应后所得滤液中加入89.4g水,则最终所得溶液中的溶质质量分数为 (3)若工业上用含Cu2S 70%的辉铜矿lOOt炼铜,并将其冶炼成上述铜的合金,(假设炼制过程中辉铜矿的损失率为10%),能炼出此铜合金的质量为 查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解  现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算: 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:
|